
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
| 时间/s | 0 | 500 | 100 0 | 150 0 |
| c(N2O5)/mol?L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A、T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 | ||
| B、500s内N2O5分解速率为2.96×10-3mol?L-1?s-1 | ||
| C、T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为50% | ||
D、达平衡后其他条件不变,将容器的体积压缩到原来的
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
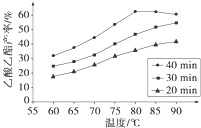 Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)
Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)| 浓H2SO4 |
| △ |
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
查看答案和解析>>
科目:高中化学 来源:志鸿系列训练必修一化学人教版 人教版 题型:008
在一定温度下将500 mL 2 mol·L-1 NaCl分为300 mL(记为A)和200 mL(记为B)两份,判断下列说法是否正确.正确的用“T”表示,错误的用“F”表示.
①A、B中NaCl物质的量浓度相同
②A中NaCl物质的量浓度较大
③A中NaCl物质的量较小
④B中NaCl物质的量浓度较小
⑤A、B的密度相同
⑥A中H2O的物质的量较大
查看答案和解析>>
科目:高中化学 来源:2012届北京市高二下期3月份月考化学试卷 题型:填空题
氨在工农业生产中应用广泛.在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下表.请回答:
|
温度/℃ |
200 |
300 |
400 |
500 |
600 |
|
氨含量/% |
89.9 |
71.0 |
47.0 |
26.4 |
13.8 |
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是______________________________________.
(2)在一定温度下,将2molN2和6 molH2通入到体积为1 L的密闭容器中,发生反应N2+ 3H2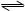 2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=_________;该温度下的平衡常数K=___________(用分数表示);欲使K增大,可以采取的措施是_______.
2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=_________;该温度下的平衡常数K=___________(用分数表示);欲使K增大,可以采取的措施是_______.
(3)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是____(选填序号字母);从化学反应速率的角度分析,提高反应速率可采取的措施是_____(选填序号字母).
a.及时分离出NH3 b.升高温度 c.增大压强 d.使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
氨在工农业生产中应用广泛.在压强为30MPa时,合成氨平衡混合气体中NH3的体积分数如下表.请回答:
| 温度/℃ | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |
(1)根据表中数据,结合化学平衡移动原理,说明合成氨反应是放热反应的原因是______________________________________.
(2)在一定温度下,将2molN2和6 molH2通入到体积为1 L的密闭容器中,发生反应N2+ 3H2![]() 2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=_________;该温度下的平衡常数K=___________(用分数表示);欲使K增大,可以采取的措施是_______.
2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)=_________;该温度下的平衡常数K=___________(用分数表示);欲使K增大,可以采取的措施是_______.
(3)从化学平衡移动的角度分析,提高H2转化率可以采取的措施是____(选填序号字母);从化学反应速率的角度分析,提高反应速率可采取的措施是_____(选填序号字母).
a.及时分离出NH3 b.升高温度 c.增大压强 d.使用催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com