
���� ��1�����λ�������ˮ�з���ˮ��������Ӧ���������コ�壬����������Ȼˮ��������ﵽ��ˮ��Ŀ�ģ�
��2��ˮ�ľ���������������ˮ����������������������ˮ�������dz�ȥˮ�еĸ����Ӻ�þ���ӣ�
��3�������ӡ�þ�������ʵ���֮���൱��CaO���ʵ�������������1Lˮ��CaO�������ɵ�ˮ��Ӳ�ȣ�
��4�������������ƽ�þ����ת��Ϊ������þ��������̼���������ת��Ϊ̼������ӣ��벿�ָ����ӽ��Ϊ̼��Ƴ��������ڸ���������ת��Ϊ̼��Ƴ�������֪n��Ca2+��+n[Ca��OH��2]=n��HCO3-��+n��Na2CO3����
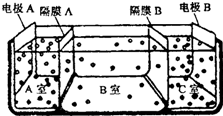
��5���ٵ缫A��ֱ����Դ���������缫B��ֱ����Դ�ĸ�����A�ҷ���������Ӧ�������������ӷŵ磬C�ҷ�����ԭ��Ӧ���������ӷŵ磬B��ʢ�ź�ˮ��Ϊ���ֵ����ԣ���������A���ƶ�����������B���ƶ���
��A���������ɣ���Һ�����ԣ�B��Ϊˮ��Ϊ���ԣ�C���м����ɣ���Һ�ʼ��ԣ�
��� �⣺��1����Ȼˮ�ھ������������м���Ļ��������������������������������ȣ��侻ˮ���õ�ԭ���ǣ����λ�������ˮ�з���ˮ��������Ӧ���������コ�壬����������Ȼˮ����������ƻ�ˮ�д��������Ľ��壬ʹ��۳��ﵽ��ˮ��Ŀ�ģ�
�ʴ�Ϊ���������������ȣ����λ�������ˮ�з���ˮ��������Ӧ���������コ�壬����������Ȼˮ����������ƻ�ˮ�д��������Ľ��壬ʹ��۳��ﵽ��ˮ��Ŀ�ģ�
��2��ˮ�ľ���������������ˮ����������������������ˮ�������dz�ȥˮ�еĸ����Ӻ�þ���ӣ�
�ʴ�Ϊ��ˮ�ľ���������������ˮ����������������������ˮ�������dz�ȥˮ�еĸ����Ӻ�þ���ӣ�
��3����ij��Ȼˮ��c��Ca2+��=1.2��10-3mol/L��c��Mg2+��=6��10-4mol/L��
��1Lˮ��CaO���ʵ����൱��1.2��10-3mol/L+6��10-4mol=1.8��10-3mol��
��1Lˮ��CaO������Ϊ1.8��10-3mol��56g/mol��1000mg/g=100.8mg
��ˮ��Ӳ��Ϊ$\frac{100.8mg}{10mg}$=10��
�ʴ�Ϊ��10�㣻
��4��10m3������Ȼˮ�У�n��Ca2+��=1.2��10-3mol/L��10000L=12mol��n��Mg2+��=6��10-4mol/L��10000l=6mol��n��HCO3-��=8��10-4mol/L��10000L=8mol��
�����������ƽ�þ����ת��Ϊ������þ��������̼���������ת��Ϊ̼������ӣ��벿�ָ����ӽ��Ϊ̼��Ƴ�����
��n[Ca��OH��2]=n��Mg2+��+$\frac{1}{2}$n��HCO3-��=6mol+4mol=10mol����m[Ca��OH��2]=10mol��74g/mol=740g��
���ڸ���������ת��Ϊ̼��Ƴ�������֪n��Ca2+��+n[Ca��OH��2]=n��HCO3-��+n��Na2CO3������n��Na2CO3��=n��Ca2+��+n[Ca��OH��2]-n��HCO3-��=12mol+10mol-8mol=14mol����m��Na2CO3��=14mol��106g/mol=1484g��
�ʴ�Ϊ��740��1484��
��5���ٵ缫A��ֱ����Դ���������缫B��ֱ����Դ�ĸ�����A�ҷ���������Ӧ�������������ӷŵ磬C�ҷ�����ԭ��Ӧ���������ӷŵ磬B��ʢ�ź�ˮ��Ϊ���ֵ����ԣ���������A���ƶ�����������B���ƶ��������ӽ���Ĥֻ��������������ͨ���������ӽ���Ĥֻ��������������ͨ�������ĤA�������ӽ���Ĥ����ĤC�������ӽ���Ĥ��
�ʴ�Ϊ������
��A���������ɣ���Һ�����ԣ�B��Ϊˮ��Ϊ���ԣ�C���м����ɣ���Һ�ʼ��ԣ�����ҺpHֵ��pHa��pHb��pHc��
�ʴ�Ϊ��pHa��pHb��pHc��
���� ������ˮ�ľ����������Լ���ˮ����Ϊ���忼�����ʷ����ᴿ���漰����ԭ����ˮ��Ӳ�ȡ���ѧ���㡢���ԭ��Ӧ�õȣ���4���м���Ϊ�״��㣬�ؼ����������ҩƷ�����ã�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2����Ư���ԣ��������ʹʯ����Һ��ɫ | |
| B�� | ������SO2����Ҫ��Դ�������ų���β�� | |
| C�� | SO2����������� | |
| D�� | SO2�ȿ����Ǻ������ʵ���������ֿ����Ǻ������ʵĻ�ԭ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 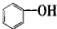 ���ڴ������ ���ڴ������ | B�� | 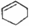 ���ڷ����廯���� ���ڷ����廯���� | ||
| C�� | 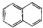 ����֬�������� ����֬�������� | D�� | CH3CH��CH3��2 ������״������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
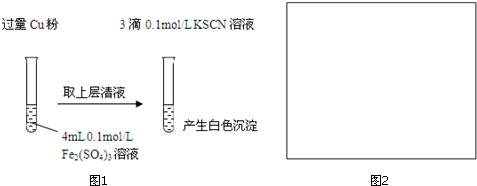
| ʵ�鷽�� | ���� | ���� |
| ����1��ȡ4mL0.1mol/L CuSO4��Һ�������еμ�3��0.1mol/L KSCN��Һ | ������ɫ���� | CuSO4��KSCN��Ӧ�����˰�ɫ���� |
| ������2��ȡȡ4mL 0.1mol/L FeSO4��Һ�������еμ�3��0.1mol/L KSCN��Һ | ���������� |
| ʵ�鷽�� | ���� |
| ��3mL 0.1mol/L FeSO4��Һ�м���1mL 8mol/Lϡ���� | ��Һ��Ϊ��ɫ������һ��ʱ�����ɫ��ʧ����Һ��Ϊ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£�pH=4.3��CH3COOH��CH3COONa�����Һ�У�c��Na+����c��CHCOO-�� | |
| B�� | NaCl��Һ��CH3COONH4��Һ�������ԣ�����Һ��ˮ�ĵ���̶���ͬ | |
| C�� | ��ͬ�¶��£���Ksp��AgCl����Ksp��Ag2CrO4������AgCl���ܽ�ȴ���Ag2CrO4 | |
| D�� | ������Һ������ˮϡ��$\frac{c��C{H}_{3}COOH��}{C��{H}^{+}��}$���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol NO | B�� | 1 mol NO2��0.05 mol O2 | ||
| C�� | 2 mol O2 | D�� | 0.25 mol O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹʪ�����-KI��ֽ����ɫ�������Ϊ���� | |
| B�� | ����������״̬���Ȼ��Ʒ�Ӧ�ɲ������� | |
| C�� | ����ֽ��AgNO3���壬Ӧ�������ɫϸ���Լ�ƿ�� | |
| D�� | ��ˮӦ����ڽ�ͷ��ƿ����ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��0.1 mol/LһԪ��BOH��Һ��pH=10������֪��Һ����BOH=B++OH- | |
| B�� | ��������ˮ���ﵽ����ƽ���ˮϡ�ͣ�����Һ�е�c��OH-����С | |
| C�� | pH=3�Ĵ����ˮϡ�ͺ�CH3COOH����̶���������볣������ | |
| D�� | �����ڴ�������Һ�еĵ���̶ȴ��ڴ�ˮ�еĵ���̶� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com