
| A、0.5mol |
| B、0.6moL |
| C、0.7mol |
| D、1.2mol |
| 3 |
| 4 |


科目:高中化学 来源: 题型:
| A、①④⑥ | B、②③⑤ |
| C、①③⑥ | D、②③⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1或3 | B、2或4 |
| C、2或3 | D、1或4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、红棕色的NO2,加压后颜色先变深后变浅 |
| B、高压比常压有利于合成SO3的反应 |
| C、加入催化剂有利于氨的合成 |
| D、工业制取金属钾Na(l)+KCl(l)?NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲溶液含有Ba2+ |
| B、乙溶液不含SO42- |
| C、丙溶液不含Cl- |
| D、丁溶液含有Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
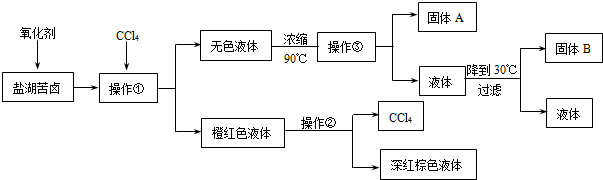

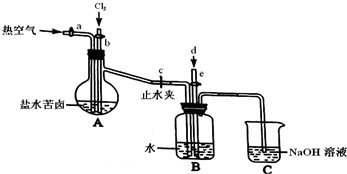

| 化学式 | Ca(OH)2 | CaSO4 | BaCO3 | BaSO4 | MgCO3 | Mg(OH)2 |
| Ksp | 1.0×10一4 | 7.1×10一5 | 8.1×10一9 | 1.08×10一10 | 3.5×10一5 | 1.6×10一11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com