
| A. | H2在负极发生氧化反应 | B. | 燃料电池的能量转化率可达100% | ||
| C. | 是一种高效、环境友好的发电装置 | D. | 供电时的总反应为:2H2+O2=2H2O |
分析 氢氧燃料电池是将化学能转变为电能的装置,工作时,通入氢气的一极为电池的负极,发生氧化反应,通入氧气的一极为电池的正极,发生还原反应,电池总反应与氢气在氧气中燃烧的化学方程式一致,产物为水,对环境无污染.
解答 解:A、由电极反应式可知,通入氧气的一极为电池的正极,发生还原反应,H2在负极发生氧化反应,故A正确;
B、燃料电池的能量转化率高,能量转换率可达80%,但是不可能为100%,故B错误;
C、氢氧燃料电池产物是水,对环境物污染,属于环境友好电池,故C正确;
D、电池总反应与氢气在氧气中燃烧的化学方程式一致,总反应为2H2+O2═2H2O,故D正确.
故选B.
点评 本题考查原电池的组成以及工作原理,题目难度不大,注意电极反应式以及电极反应的产物.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳的结构式:O=C=O | B. | 氯离子的结构示意图: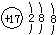 | ||
| C. | 钙离子的电子式:Ca2+ | D. | 溴化氢分子的电子式: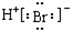 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气(混合物)、C2H5OH(醇)、H2SO4(离子化合物)、液氨(电解质) | |
| B. | CO2(非电解质)、NH4Cl(铵盐)、HNO3(含氧酸)、NaOH(强电解质) | |
| C. | HCl(共价化合物)、CH3COOH(羧酸)、Na2O2(碱性氧化物)、CH3I(卤代烃) | |
| D. | NO2(酸性氧化物)、CH3CHO(有机物)、CO(有机物)、CH3COOCH3(酯) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液:Cu2+、H+、Cl-、NO3- | |
| B. | 能使酚酞试液呈红色的溶液:Na+、K+、Cl-、CO32- | |
| C. | 能与金属Fe反应放出H2的溶液中:Na+、Cl-、SO42-、NO3- | |
| D. | 含有HCO3-的溶液中:K+、OH-、NO3-、Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | x=0.4a,2Fe2++Cl2═2Fe3++2Cl- | |
| B. | x=0.6a,2Br-+Cl2═Br2+2Cl- | |
| C. | x=2a,2Fe2++2Br-+2Cl2═Br2+2Fe3++4Cl- | |
| D. | x=1.5a,2Fe2++4Br-+3Cl2═2Br2+2Fe3++6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1mol H2O的体积为22.4L | |
| B. | 1mol•L-1的氯化钠溶液是指此溶液中含有1mol NaCl | |
| C. | 从1L 1mol•L-1的NaCl溶液中取出100mL溶液,其物质的量浓度变为0.1mol•L-1 | |
| D. | 以g•mol-1为单位时,在数值上摩尔质量与相对分子质量或相对原子质量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2和H2SO4;Cu(OH)2和CH3COOH | B. | Ba(OH)2和Na2SO4;Ba(OH)2和CuSO4 | ||
| C. | NaOH和H2SO4;NaOH和NaHSO4 | D. | Na2CO3和盐酸;NaHCO3和盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com