
A.氨和水在氧化还原反应中只能作还原剂
B.氟和氧参加的氧化还原反应都是置换反应
C.氮的非金属性比氧弱,氧的非金属性比氟弱
D.按氮、氧、氟顺序,它们的最高价氧化物的水化物的酸性依次增强
科目:高中化学 来源: 题型:阅读理解



查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
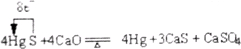
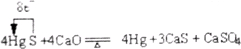
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:021
A.氨和水在氧化还原反应中只能做还原剂
B.氟和氧参加的氧化还原反应都是置换反应
C.氮的非金属性比氧弱,氧的非金属性比氟弱
D.按氮、氧、氟的顺序,它们最高价氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:021
对比以下两个化学反应:2F2+2H2O═4HF+O2,4NH3+3O2![]() 2N2+6H2O(纯氧中),可以得到的结论是( )
2N2+6H2O(纯氧中),可以得到的结论是( )
A.氨和水在氧化还原反应中只能做还原剂
B.氟和氧参加的氧化还原反应都是置换反应
C.氮的非金属性比氧弱,氧的非金属性比氟弱
D.按氮、氧、氟的顺序,它们最高价氧化物对应的水化物的酸性依次增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com