
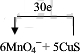
已知:2KMnO4+16HCl==2KCl+2MnCl2+5Cl2↑+8H2O,K2Cr2O7+14HCl==2KCl+2CrCl3+3Cl2↑+7H2O,MnO2+4HClMnCl2+Cl2↑+2H2O,
其中,KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6mol/L)反应,MnO2需和浓盐酸(>8mol/L)反应。根据以上信息,下列结论中不正确的是( )
A.上述反应既属于氧化还原反应,又属于离子反应
B.生成1molCl2转移电子数均为2NA
C.盐酸浓度越大,Cl—的还原性越强
D.氧化性:KMnO4 >K2Cr2O7>Cl2> MnO2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
(2012?上海)图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O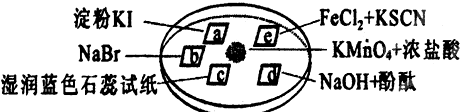 对实验现象的“解释或结论”正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com