
| A、只有AgBr沉淀生成 |
| B、AgCl和AgBr沉淀等量生成 |
| C、AgCl沉淀少于AgBr沉淀 |
| D、AgCl沉淀多于AgBr沉淀 |


科目:高中化学 来源: 题型:
| A、某特定反应的平衡常数仅是温度的函数 |
| B、催化剂不能改变平衡常数的大小 |
| C、平衡常数发生变化,化学平衡必定发生移动 |
| D、化学平衡发生移动,平衡常数必发生改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
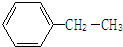
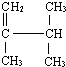
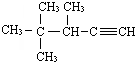
 表示的分子式
表示的分子式查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化铵晶体溶于水中 |
| B、NO(g)和O2(g)反应生成NO2(g) |
| C、碘晶体受热升华 |
| D、BaCO3(s)分解为BaO(s)和CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
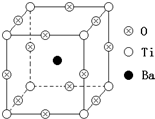 如图所示为PTC元件(热敏电阻)的主要成分--钡钛矿晶体结构,该结构是具有代表性的最小重复单位.该晶体经X射线分析鉴定,重复单位为正方体,边长a=403.1pm,顶点位置为Ti4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占.
如图所示为PTC元件(热敏电阻)的主要成分--钡钛矿晶体结构,该结构是具有代表性的最小重复单位.该晶体经X射线分析鉴定,重复单位为正方体,边长a=403.1pm,顶点位置为Ti4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占.查看答案和解析>>
科目:高中化学 来源: 题型:
 -CH2(CH2)3CH3、
-CH2(CH2)3CH3、 -CH(CH3)(CH2)2CH3、
-CH(CH3)(CH2)2CH3、 -CH2CH(CH3)CH2CH3、
-CH2CH(CH3)CH2CH3、 -CH2CH2CH(CH3)CH3,写出另外3种的结构简式:
-CH2CH2CH(CH3)CH3,写出另外3种的结构简式:查看答案和解析>>
科目:高中化学 来源: 题型:
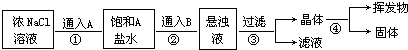
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com