
����Ŀ����������ͼʾ����������ȷ����
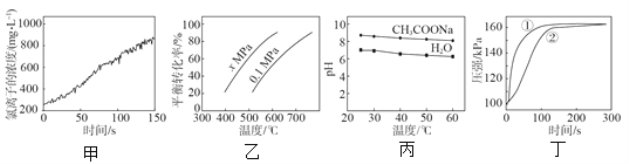
A.����������ˮ���չ�����������Ũ�ȵı仯���ߣ��ƶϴ�����ֽ������� HCl �� O2
B.���� C4H10(g)![]() C4H8(g) + H2(g)��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ���ߣ��ƶϸ÷�Ӧ��H��0��x��0.1
C4H8(g) + H2(g)��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ���ߣ��ƶϸ÷�Ӧ��H��0��x��0.1
C.���� 0.03g þ���ֱ��� 2 mL 2 mol/L ����ʹ��ᷴӦ�������ܱ�����������ѹǿ��ʱ��ı仯���ߣ��ƶϢٴ���������þ���ķ�Ӧ
D.���� 0.5 mol/L CH3COONa ��Һ��ˮ�� pH ���¶ȵı仯���ߣ�˵�����¶����ߣ�CH3COONa ��Һ�� c(OH-)��С
���𰸡�C
��������
A����������ˮ�д��ڿ��淴ӦCl2+H2OH++Cl-+HClO���Ӽ�ͼ�п��Կ��������Ź��յIJ��Ͻ��У�������ˮ��c(Cl-)���������ɴ˿��ƶϴ�����ֽ������� HCl�������ܿ϶��Ƿ���O2���ɣ�A����ȷ��
B������ͼ�п��Կ����������¶ȣ�C4H10(g)![]() C4H8(g) + H2(g)��ƽ��ת���������������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ��H��0��ѹǿ��0.1MPa��ΪxMPaʱ��ƽ��ת�������������ƽ�������ƶ�������ӦΪ��Сѹǿ��x<0.1��B����ȷ��
C4H8(g) + H2(g)��ƽ��ת���������������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ��H��0��ѹǿ��0.1MPa��ΪxMPaʱ��ƽ��ת�������������ƽ�������ƶ�������ӦΪ��Сѹǿ��x<0.1��B����ȷ��
C������ΪһԪǿ�ᣬ����ΪһԪ���ᣬ2 mL 2 mol/L ����ʹ����У�������c(H+)����0.03g þ����Ӧ�����ʴ���ͬʱ���ڲ������������࣬���ղ�����H2������ȣ��Ӷ�ͼ�п��Կ����ٵķ�Ӧ���ʿ죬�ɴ˿��ƶϢٴ���������þ���ķ�Ӧ��C��ȷ��
D��0.5 mol/L CH3COONa ��Һ��ˮ�У���������ƽ�⣺CH3COO-+H2OCH3COOH+OH-��H2OH++OH-��CH3COO-��ˮ���ˮ�ĵ��붼�����ȹ��̣������¶�ƽ�������ƶ�������CH3COONa��Һ��c(OH-)����D����ȷ��
��ѡC��


 ̽���빮�̺��Ͽ�ѧ����������ϵ�д�
̽���빮�̺��Ͽ�ѧ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ��ѧ����Ԫ��ԭ�ӽṹ���������±���ʾ
Ԫ�� | �ṹ������ |
A | Ԫ��A�ڵ��������м����Ӱ뾶��С |
B | Bԭ���������������ڲ��������0.6 |
C | ʹ����㷺�Ľ���Ԫ��C���γ������Ȼ������Է�������֮��Ϊ35.5 |
D | Ԫ��D��Bͬ���壬�Ҵ���������D���������ϼ� |
E | Ԫ��E�����ڱ���λ����A�壬������Ϊ����������A��Ҳ��һ������ |
F | Ԫ��F��Bͬ���ڣ�������������ˮ������A��B������������ˮ������ܷ�Ӧ |
(1)Ԫ��C�����ڱ��е�λ����____Ԫ�أ�Ԫ��E�γɵ�һ�ּ�������֧������Ԫ��E������A������һ�۵㣬�����ӵĽṹʾ��ͼΪ___��
(2)Ԫ��E��D����ԭ�Ӹ�����2��1��1��1�γ����ֻ�����X��Y������X��Y���������ʵ�ʵ�鷽��Ϊ __��E��B�γɵ�һ�ֻ�����Z��X��Y�е�һ�ֵ���������ͬ���ܷ�����ѧ��Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ��___(����Ӧ��ѧʽ��ʾ)��
(3)�뻭��������F2B2�ĵ���ʽ��_____���û������к��еĻ�ѧ��������___��
(4)Ԫ��A��Ԫ��F��ȣ������Խ�ǿ����_________ (��Ԫ�ط��ű�ʾ)�����б�����ȷ����֤����һ��ʵ����___(����ĸ����)��
a����Ӧ�������ᷴӦʱ��ÿ��Aԭ�ӱ�ÿ��Fԭ��ʧ���Ӷ�
b����Ӧ������ͬŨ�����ᷴӦʱ��F��A���ҵö�
c��A���������۵��F���������۵��
d��F�ɽ�A��������Һ���û�����
e������������Ӧ��ˮ����ļ���F��A��ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�����ԭ�ϵĽṹ��ʽ��ͼ��ʾ�����й��ڸ��л����˵����ȷ���ǣ� ��
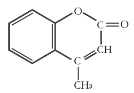
A.1 mol����������ܺ�5mol H2�����ӳɷ�Ӧ
B.��ʹ����KMnO4��Һ��ɫ���ܷ����ӳɷ�Ӧ��ȡ����Ӧ
C.�÷���������ԭ�Ӷ����ܹ�ƽ��
D.�����ʵķ���ʽΪC10H10O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 100��ʱ���� 0.40 mol NO2 ������� 2 L ���ܱ������У��������·�Ӧ��2NO2(g)![]() N2O4(g) H < 0����ⷴӦ����������ݣ�
N2O4(g) H < 0����ⷴӦ����������ݣ�
ʱ��/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
����˵����ȷ����
A.0~20 s �ڣ�v(NO2) = 0.005 mol��L-1.s-1
B.��������Ӧ�� 120��ʱ���У���Ӧ�� 80 s ʱ��n(N2O4) < 0.08 mol
C.��������ʼʱ���� NO2 �������� 0.80 mol����ƽ��ʱ NO2 ת���ʽ�����
D.59 s ʱ��c(NO2)һ������ 0.12 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ȡpH=2�����ֶ�Ԫ��H2A��H2B��1ml���ֱ��ˮϡ�ͣ����pH���ˮϡ�ͱ�������ͼ��ʾ��ϵ���������й���������ȷ����
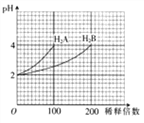
A. H2B����
B. NaHAˮ��Һ�У�c(Na+)+c(H+)=2c(A2��)+c(OH��)
C. �������ʵ�����NaHA��NaHB�Ļ����Һ�У�c(Na+)=c(A2��)+c(HB��)+c(B2��)+c(H2B)
D. pH=10��NaHB��Һ�У�c(Na+)>c(HB��)>c(B2��)>c(OH��)>c(H2B)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ͼΪʵ�����Ʊ����ռ�����HCl��װ�á�
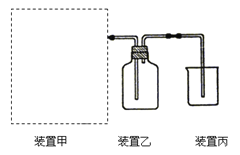
�� �Ʊ�HCl����ҩƷΪŨ�����Ũ���ᣬ������װ��Ӧѡ����ͼ�е� ��

�� ���������Ũ�����Ũ�����Ʊ�HCl�����ԭ�� ��
�� װ�ñ��������չ�����HCl���壬Ϊ��ֹ���������ձ���Ӧ��װ��ˮ�� ��
��2������Ϊ����ȡ����Ӧ��̽��ʵ�顣
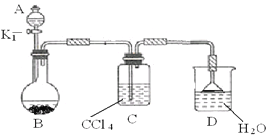
������ͼ��ʾ��װ��ͼ���Ӻø�������
������װ�õ������ԡ�
����A�м��������ı���Һ��Ļ��Һ�壬��B�м����������ۣ�������Ƥ������K1����ʼ���з�Ӧ�������������Һ�ر�K1��
д��B�з�����Ӧ�Ļ�ѧ����ʽ ��װ��C�������� ��
����Ӧ���������Թ�ȡ����D�е���Һ������
�������Լ���������֤��B�е�ȡ����Ӧ�Ѿ�������
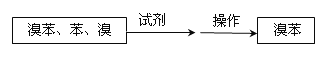
����B�еĹ�Һ���������ˣ������Һ���������ͼ�������ƺ��б�������屽�������Լ�Ϊ ����������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1000 mol/L��NaOH����Һ�ζ�20.00 mL0.1000 mol/L��HCl��Һ���ζ�������ͼ�������й�˵����ȷ����( )

A.ָʾ����ɫʱ��˵����Ӧ���ᡢ��ǡ�õ����ʵ�����Ӧ
B.���ﵽ�ζ��յ�ʱ�Ŵ���c(Na+)+c(H+)=c(Cl-)+c(OH-)
C.�ﵽ�ζ��յ�ʱ���ü�����ָʾ������NaOH��Һ������÷�̪��
D.��֪H+(aq)+OH-(aq)=H2O(l)��H=-57.3 kJ/mol�������ζ�ǡ���к�ʱ���ų�114.6J������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����þ������ pH��8.4 �ı��� NaHCO3 ��Һ�У�þ������������� a��һ��ʱ��������ɫ����b��������������ʵ�飺
������ a ͨ������ʯ��ˮ������ǣ��̶�ͨ������ NaOH ��Һ����ͨ�����Һ���������ݣ���ȼ����������������
��������� b �м���������ϡ���ᣬ������ȫ�ܽ⣬�Ҳ�����ɫ���ݡ�����˵������ȷ����
A.���� NaHCO3 ��Һ�У�c(![]() )< c(H2CO3)
)< c(H2CO3)
B.���� b �� MgCO3
C.���� a ��� CO2 �� H2
D.CO2 ������ ![]() ˮ�ⱻ�ٽ�������
ˮ�ⱻ�ٽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ�������������

A.��ͼ�����жϣ���T1>T2����ӦA(g)+ B(g)![]() 2C(g)����H<0
2C(g)����H<0
B.ͼ�ұ�ʾѹǿ�Կ��淴Ӧ2A(g)+2 B(g)![]() 3C(g)+D��s����Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
3C(g)+D��s����Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
C.����ͼ��������ȥCuSO4��Һ�е�Fe3+��������Һ�м�������NaOH��Һ������pH��4
D.ͼ����ʾ��0.1mol/L������ζ�20mL 0.1mol/LNaOH��Һ����ҺpH�������������ı仯
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com