
| A、将等体积pH=4的盐酸和醋酸稀释到pH=5的溶液,醋酸所加的水量少 |
| B、盐酸和醋酸都可用相应的钠盐和浓硫酸反应制取 |
| C、相同pH的等体积盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸pH变大,盐酸pH不变 |
| D、相同pH的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
| 选项 | X | Y | Z | 箭头上为反应条件 | 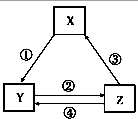 |
| A | NO | NO2 | HNO3 | ②加H2O | |
| B | Al | NaAlO2 | AlCl3 | ③电解 | |
| C | Fe | FeCl2 | FeCl3 | ①通入少量Cl2 | |
| D | NaOH | NaHCO3 | NaCl | ④依次通入CO2、NH3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲多 | B、乙多 |
| C、一样多 | D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
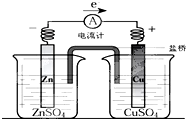
| A、铜是阳极,铜片上有气泡产生 |
| B、正极附近的SO42-离子浓度逐渐增大 |
| C、电流从锌片经导线流向铜片 |
| D、铜离子在铜片表面被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、M为非电解质 |
| B、M是强电解质 |
| C、M为一种盐 |
| D、M是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性:HClO4>H3PO4>H2SO4 |
| B、氢化物的稳定性:H2S>HF>H2O |
| C、碱性:Al(OH)3>Mg(OH)2>NaOH |
| D、氧化性:F2>C12>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.8 g的NH4+离子中含有的电子数为NA |
| B、常温常压下,11.2 L氧气所含的原子数为NA |
| C、常温常压下,48 g O3和O2的混合物含有的氧原子数为3NA |
| D、2.4 g金属镁变为镁离子时失去的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com