
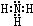 ;
; ,64gB的物质的量是2mol,2mol肼和双氧水完全反应生成氮气和水放出3000kJ的热量,则1mol肼和双氧水反应生成氮气和水放出1500kJ燃料,该反应的热化学方程式N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500 kJ/mol;
,64gB的物质的量是2mol,2mol肼和双氧水完全反应生成氮气和水放出3000kJ的热量,则1mol肼和双氧水反应生成氮气和水放出1500kJ燃料,该反应的热化学方程式N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500 kJ/mol;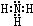 ;
; ;N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500 kJ/mol;
;N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500 kJ/mol;

科目:高中化学 来源: 题型:
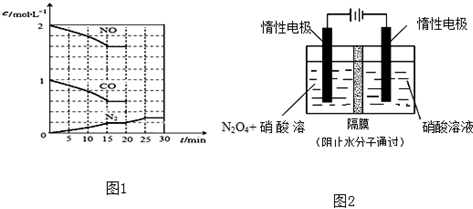
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
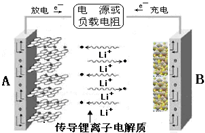 锂离子电池是具有电压高、能量密度大、循环性能好等突出优点的高效绿色产品.某锂离子电池的结构如右图所示,以石墨化的碳、氧化钴锂(LiCoO2)为电极,当充电时,阳极上发生的电极反应为LiCoO2-xe-=Li1-xCoO2+xLi+,总反应式为LiCoO2+6C=Li1-xCoO2+LixC6.
锂离子电池是具有电压高、能量密度大、循环性能好等突出优点的高效绿色产品.某锂离子电池的结构如右图所示,以石墨化的碳、氧化钴锂(LiCoO2)为电极,当充电时,阳极上发生的电极反应为LiCoO2-xe-=Li1-xCoO2+xLi+,总反应式为LiCoO2+6C=Li1-xCoO2+LixC6.| 充电 |
| 放电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、鸡蛋清溶液中加入饱和Na2SO4溶液,有沉淀产生,再加入大量水,沉淀不溶解 |
| B、乙醇溶液常用于医疗消毒是因为它能使细菌蛋白体发生变性 |
| C、在临床上解救误服重金属盐中毒的病人时,常要求病人服用大量牛奶或豆浆 |
| D、皮肤、指甲不慎沾上浓硝酸会出现黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、F2+H2O |
| B、Li+O2(条件点燃) |
| C、CO2+Mg |
| D、NO2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、②④⑥ |
| C、①⑤⑥ | D、①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com