
|
自然界中某些矿物的形成过程会发生如下反应: 14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,下列说法正确的是 | |
A. |
FeS2只作还原剂,CuSO4只作氧化剂 |
B. |
5 mol FeS2发生反应,有21 mol电子转移 |
C. |
产物中的SO |
D. |
Cu2S是还原产物 |
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 1.86 | 1.52 | 0.66 | 1.43 | 0.77 | 1.10 | 0.99 | 2.31 | 0.70 | 0.64 |
| 最高价态 | +1 | +1 | -- | +3 | +4 | +5 | +7 | +1 | +5 | -- |
| 最低价态 | -- | -- | -2 | -- | -4 | -3 | -1 | -- | -3 | -1 |
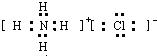
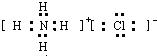
查看答案和解析>>
科目:高中化学 来源: 题型:
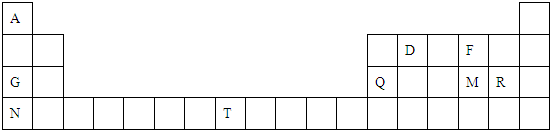
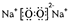
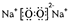


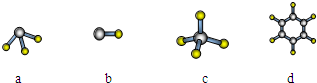
查看答案和解析>>
科目:高中化学 来源: 题型:
自然界中某些矿物的形成过程会发生如下反应:
![]() ,下列说法正确的是
,下列说法正确的是
A. FeS2只作还原剂,CuSO4只作氧化剂 B. 5mol FeS2发生反应,有21mol电子转移
C. 产物中的![]() 离子都是氧化产物 D. Cu2S是还原产物
离子都是氧化产物 D. Cu2S是还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com