
 ,违背了泡利不相容原理.
,违背了泡利不相容原理.分析 A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大,A元素原子的核外p电子数比s电子数少1,电子排布为1s22s22p3,故A为N元素;B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期,则其电子排布为1s22s22p63s2,故B为Mg;C处于第三周期,C原子核外所有p轨道全满或半满,最外层排布为3s23p3,故C为P元素;D处于第三周期,D元素的主族序数与周期数的差为4,处于ⅦA族,故D为Cl元素;E是前四周期中电负性最小的元素,则E为K元素;F在周期表的第四周期第7列,则F为Mn,据此解答.
解答 解:A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大,A元素原子的核外p电子数比s电子数少1,电子排布为1s22s22p3,故A为N元素;B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期,则其电子排布为1s22s22p63s2,故B为Mg;C处于第三周期,C原子核外所有p轨道全满或半满,最外层排布为3s23p3,故C为P元素;D处于第三周期,D元素的主族序数与周期数的差为4,处于ⅦA族,故D为Cl元素;E是前四周期中电负性最小的元素,则E为K元素;F在周期表的第四周期第7列,则F为Mn.
(1)A为N元素,核外电子排布式为1s2ns2np3,基态原子中能量最高的电子,处于2p能级,有3个电子,其电子云在空间有3个方向,原子轨道呈纺锤形,
故答案为:3;纺锤;
(2)某同学根据上述信息,推断B基态原子的核外电子排布为 ,该同学所画的电子排布图中3s能级,2个电子自旋方向相同,违背了泡利不相容原理,
,该同学所画的电子排布图中3s能级,2个电子自旋方向相同,违背了泡利不相容原理,
故答案为:泡利不相容;
(3)F为Mn元素,处于周期表中第四周期ⅦB族,属于d区元素,核外有25个电子,运动状态均不相同,有25种不同运动状态,价电子排布式为:3d54s2,
故答案为:ⅦB;d;25;3d54s2;
(4)PCl3中心原子P原子成3个σ键,P原子价层电子对是为3+1=4,含有1对孤对电子对,杂化轨道数为4,杂化方式为sp3,其空间构型为三角锥;
E为K元素,检验K元素的方法是:焰色反应,
故答案为:sp3;三角锥形;焰色反应.
(5)HN3是一种弱酸,可部分电离出H+和N3-.配体含有孤对电子,配合物[Co(N3)(NH3)5]SO4中的配体是:N3-、NH3,钴离子的配位数是6,
故答案为:N3-、NH3;6.
点评 本题是对物质结构与性质的考查,涉及核外电子运动与排布规律、杂化轨道理论、分子结构等,难度中等,推断元素是解题的关键,注意对基础知识的掌握.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯气可用于自来水消毒 | B. | 甲醛可用作食品防腐剂 | ||
| C. | 碳酸钠可用来治疗胃酸过多 | D. | 铝制容器可长期存放碱性物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH5的电子式为: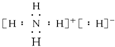 | |
| B. | 分馏、干馏、裂化都是化学变化 | |
| C. | 2-甲基-1-丁烯的结构简式: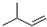 | |
| D. | NaHSO4和Na2O2的阴、阳离子个数比均为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B、C三种元素形成的化合物中肯定只含共价键 | |
| B. | A、C形成的化合物中只有A-C键 | |
| C. | 工业上生产单质D可用海水作原料获得 | |
| D. | 化合物DC与化合物EC2中化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅和氯化镁熔化 | B. | 碘和氯化铵受热变成气体 | ||
| C. | 水和干冰的气化 | D. | 氯化钠和氯化氢溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二者燃烧时现象完全相同 | |
| B. | 点燃前都不需要验纯 | |
| C. | 甲烷燃烧火焰呈淡蓝色,乙烯燃烧火焰较明亮 | |
| D. | 二者燃烧时都有黑烟生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸 | B. | 加入NaOH溶液 | C. | 加入澄清石灰水 | D. | 通入CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
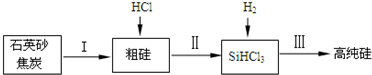
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
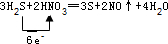 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com