
 ;该反应的反应类型为酯化反应或取代反应
;该反应的反应类型为酯化反应或取代反应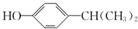
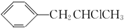 为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):
为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):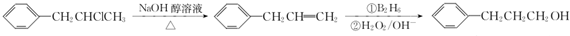 .
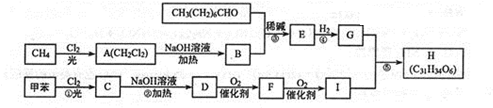
. 分析 A是烃类,其相对分子质量为56,则$\frac{56}{12}$=4…8,可知A的分子式为C4H8,结合反应信息可知A属于烯烃,则B属于饱和一元醇,C为饱和一元醛,D为饱和一元羧酸,D分子的核磁共振氢谱上有3组峰且峰面积之比为6:1:1,则D的结构简式为(CH3)2CHCOOH,逆推可知C为(CH3)2CHCHO,B为(CH3)2CHCH2OH,A为(CH3)2C=CH2.D和F反应生成一元芳香酯G,则F为芳香醇,E可以发生银镜反应,含有-CHO,1molE和1molF分别完全燃烧时,F生成的水比E的多2 mol,说明E中还含有碳碳双键,在催化剂存在条件下1mol E与2mol H2反应可以生成F,F分子中含有苯环但无甲基,F的分子式为C9H12O,可推知E为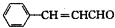 ,F为
,F为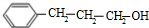 ,则G为
,则G为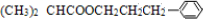 .
.
解答 解:A是烃类,其相对分子质量为56,则$\frac{56}{12}$=4…8,可知A的分子式为C4H8,结合反应信息可知A属于烯烃,则B属于饱和一元醇,C为饱和一元醛,D为饱和一元羧酸,D分子的核磁共振氢谱上有3组峰且峰面积之比为6:1:1,则D的结构简式为(CH3)2CHCOOH,逆推可知C为(CH3)2CHCHO,B为(CH3)2CHCH2OH,A为(CH3)2C=CH2.D和F反应生成一元芳香酯G,则F为芳香醇,E可以发生银镜反应,含有-CHO,1molE和1molF分别完全燃烧时,F生成的水比E的多2 mol,说明E中还含有碳碳双键,在催化剂存在条件下1mol E与2mol H2反应可以生成F,F分子中含有苯环但无甲基,F的分子式为C9H12O,可推知E为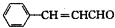 ,F为
,F为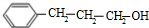 ,则G为
,则G为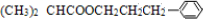 .
.
(1)B为(CH3)2CHCH2OH,用系统命名法命名为:2-甲基-1-丙醇,E为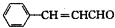 ,官能团的名称是:碳碳双键、醛基,
,官能团的名称是:碳碳双键、醛基,
故答案为:2-甲基-1-丙醇;碳碳双键、醛基;
(2)由上述分析可知,A的结构简式是(CH3)2C=CH2,B、C、D分别含有羟基、醛基、羧基,可以用新制氢氧化铜悬浊液鉴别,
故答案为:(CH3)2C=CH2;新制氢氧化铜悬浊液;
(3)D与F反应的化学方程式为: ,该反应的反应类型为酯化反应或取代反应,
,该反应的反应类型为酯化反应或取代反应,
故答案为: ;酯化反应或取代反应;
;酯化反应或取代反应;
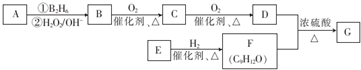
(4)满足下列条件的F(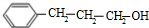 )的同分异构体:①能与NaOH溶液反应,说明含有酚羟基,②分子中有2个-CH3,可以含有2个取代基为-OH、-CH(CH3)2,有邻、间、对3种,可以含有3个取代基为-OH、-CH3、-CH2CH3,而-OH、-CH3有邻、间、对3种位置,对应的-CH2CH3分别有4种、4种、2种位置,故符合条件的共有13种,其中核磁共振氢谱有5组峰的结构简式为:
)的同分异构体:①能与NaOH溶液反应,说明含有酚羟基,②分子中有2个-CH3,可以含有2个取代基为-OH、-CH(CH3)2,有邻、间、对3种,可以含有3个取代基为-OH、-CH3、-CH2CH3,而-OH、-CH3有邻、间、对3种位置,对应的-CH2CH3分别有4种、4种、2种位置,故符合条件的共有13种,其中核磁共振氢谱有5组峰的结构简式为: ,
,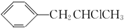 先在氢氧化钠醇溶液、加热条件下发生消去反应生成
先在氢氧化钠醇溶液、加热条件下发生消去反应生成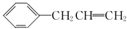 ,
,
然后经过①B2H6、②H2O2/OH-作用生成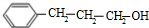 ,合成路线流程图为:
,合成路线流程图为: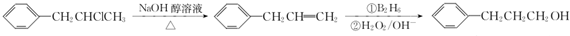 ,
,
故答案为:13; ;
;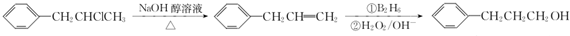 .
.
点评 本题考查有机物推断与合成,需要学生对给予的信息进行利用,是常见题型,侧重考查学生的分析推理能力,熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:选择题
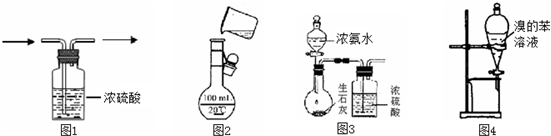
| A. | 图1用于除氯气中的水蒸气 | B. | 图2进行溶液的定容 | ||
| C. | 图3用于制取干燥的氨气 | D. | 图4用于溴与苯的分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(l)△H1 2H2(g)+O2(g)═2H2O(g)△H2 | |
| B. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | H2(g)+Cl2(g)═2HCl(g)△H1$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
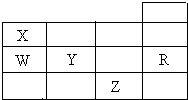 如表为元素周期表前四周期的一部分,X、W、Y、R、Z分别代表元素符号,其中R元素的原子每个电子层都达到稳定结构.下列叙述中正确的是( )
如表为元素周期表前四周期的一部分,X、W、Y、R、Z分别代表元素符号,其中R元素的原子每个电子层都达到稳定结构.下列叙述中正确的是( )| A. | XZ3是平面正三角形分子 | |
| B. | 钠与X形成的化合物Na3X和NaX3都是含有共价键的离子晶体 | |
| C. | W与Y元素的最高价氧化物对应的水化物酸性前者弱于后者 | |
| D. | X的氢化物比W的氢化物稳定,但沸点前者比后者低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
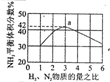 |  | 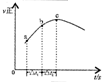 | 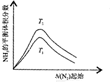 |
| 根据图中a点数据计算N2的平衡体积分数:14.5% | 表示从通入原料开始,随温度不断升高,NH3物质的量变化的曲线示意图 | 向绝热恒容器中通入N2和H2,△t1=△t2时,N2的转化率:a-b段大于b-c段 | 图中T2<T1 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
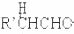 $\stackrel{稀碱}{→}$
$\stackrel{稀碱}{→}$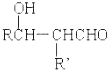
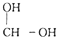 -OH$\stackrel{-H_{2}O}{→}$RCHO
-OH$\stackrel{-H_{2}O}{→}$RCHO .
. .
.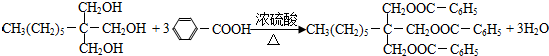 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
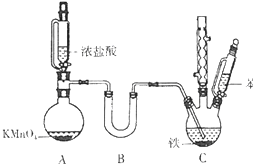 氯苯是重要的有机化工原料.实验室制备氯苯的反应原理、实验装置如图所示(加热装置已略去):
氯苯是重要的有机化工原料.实验室制备氯苯的反应原理、实验装置如图所示(加热装置已略去):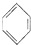 +Cl2$\stackrel{FeCl_{3}}{→}$
+Cl2$\stackrel{FeCl_{3}}{→}$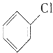 +HCl
+HCl| 沸点(℃) | 密度(g•mL-1) | 溶解性 | |
| 苯 | 80.1 | 0.88 | 难溶于水 |
| 氯苯 | 132.2 | 1.10 | 难溶于水,易溶于有机溶剂 |
| 对二氯苯 | 173.4 | 1.46 | 难溶于水,易溶于有机溶剂 |
| 邻二氯苯 | 180.4 | 1.30 | 难溶于水,易溶于有机溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +CO$→_{△}^{AlCl_{3},HCl}$
+CO$→_{△}^{AlCl_{3},HCl}$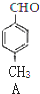 $→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$
$→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$ $→_{浓硫酸△}^{CH_{3}OH}$E
$→_{浓硫酸△}^{CH_{3}OH}$E .
.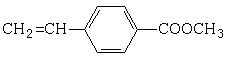 B.
B.
 D
D
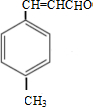
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com