
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚĪļÖŹ×é³ÉµÄĖµ·ØÖŠ£¬ÕżČ·µÄŹĒ
A.Ėį”¢¼ī”¢ŃĪæÉÄܶ¼²»ŗ¬½šŹōŌŖĖŲ
B.ŗ¬ŃõŌŖĖŲµÄ»ÆŗĻĪļŅ»¶ØŹĒŃõ»ÆĪļ
C.µ„ÖŹ²»Ņ»¶ØÖ»ŗ¬Ņ»ÖÖŌŖĖŲ
D.Ėį”¢¼īÖŠŅ»¶Øŗ¬Ēā£¬ŃĪŅ»¶Ø²»ŗ¬Ēā

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”涞Ńõ»ÆĀČ(ClO2£¬»ĘĀĢÉ«Ņ×ČÜÓŚĖ®µÄĘųĢå)ŹĒŅ»ÖÖ°²Č«ĪČ¶Ø”¢øߊ§µĶ¶¾µÄĻū¶¾¼Į”£¹¤ŅµÉĻĶعż¶čŠŌµē¼«µē½āĀČ»Æļ§ŗĶŃĪĖįµÄ·½·ØÖʱø£¬ĘäŌĄķČēĶ¼ĖłŹ¾:
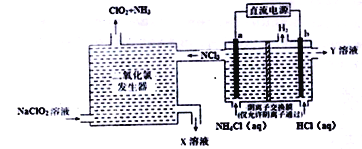
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. bµē¼«½ÓµēŌ“µÄøŗ¼«£¬ŌŚb¼«ĒųĮ÷³öµÄYČÜŅŗŹĒĻ”ŃĪĖį
B. ¶žŃõ»ÆĀČ·¢ÉśĘ÷ÖŠÅųöµÄXČÜŅŗÖŠČÜÖŹÖ÷ŅŖĪŖNaClŗĶNaOH
C. µē½ā¹ż³ĢÖŠ¶žŃõ»ÆĀČ·¢ÉśĘ÷ÖŠ²śÉś2.24L(±ź×¼×“æö)NH3£¬Ōņb¼«²śÉś0.6gH2
D. µē½ā³Ųa¼«µÄµē¼«·“Ó¦Ź½ĪŖNH4+-6e-+4OH-+3Cl-=NCl3+4H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒŹµŃéŹŅÖĘČ”SO2²¢ŃéÖ¤SO2µÄijŠ©ŠŌÖŹµÄ×°ÖĆ£¬ŹŌ»Ų“š

ŹŌ»Ų“š£ŗ
£Ø1£©¢ŚÖŠµÄŹµŃéĻÖĻóĪŖ______________”£
£Ø2£©¢ÜÖŠµÄŹµŃéĻÖĻóĪŖ______________£¬“ĖŹµŃéĖµĆ÷SO2ÓŠ____________ŠŌ£®
£Ø3£©¢ŻÖŠµÄŹµŃéĻÖĻóĪŖ____________£¬“ĖŹµŃéĖµĆ÷SO2ÓŠ________ŠŌ£®
£Ø4£©¢ŽµÄ×÷ÓĆŹĒ___________£¬·“Ó¦·½³ĢŹ½ŹĒ_____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©NaClOČÜŅŗŌŚ¼īŠŌĢõ¼žĻĀ½«CN£Ńõ»Æ³ÉĪŽ¶¾µÄĢ¼ĖįøłĄė×ÓŗĶN2£¬øĆ·“Ó¦Ąė×Ó·½³ĢŹ½________________________________”£
£Ø2£©NH3”¤H2OµÄµēĄė·½³ĢŹ½ĪŖNH3”¤H2O![]() NH4£«£«OH££¬ŹŌÅŠ¶ĻČÜÓŚĖ®ŗ󣬊Ī³ÉµÄŗĻĄķ½į¹¹ŹĒ________”£(ĢīĶ¼ÖŠµÄ×ÖÄø)
NH4£«£«OH££¬ŹŌÅŠ¶ĻČÜÓŚĖ®ŗ󣬊Ī³ÉµÄŗĻĄķ½į¹¹ŹĒ________”£(ĢīĶ¼ÖŠµÄ×ÖÄø)

£Ø3£©°ŃCoCl2ČÜÓŚĖ®ŗó¼Ó°±Ė®Ö±µ½ĻČÉś³ÉµÄCo(OH)2³ĮµķÓÖČܽāŗó£¬ŌŁ¼Ó°±Ė®£¬Ź¹Éś³É[Co(NH3)6]2£«£¬“ĖŹ±ĻņČÜŅŗÖŠĶØČėæÕĘų£¬µĆµ½µÄ²śĪļÖŠÓŠŅ»ÖÖĘä×é³ÉæÉÓĆCoCl3”¤5NH3±ķŹ¾£¬CoµÄÅäĪ»ŹżŹĒ6”£°Ń·ÖĄė³öµÄCoCl3”¤5NH3ČÜÓŚĖ®ŗóĮ¢¼“¼ÓĻõĖįŅųČÜŅŗ£¬ŌņĪö³öAgCl³Įµķ”£¾²ā¶Ø£¬Ćæ1molCoCl3”¤5NH3ֻɜ³É2molAgCl£¬CoCl3”¤5NH3ÖŠCo»ÆŗĻ¼ŪĪŖ__________£¬ĒėŠ“³ö±ķŹ¾“ĖÅäŗĻĪļ½į¹¹µÄ»ÆѧŹ½£ŗ______________”£
£Ø4£©H2O”¢H2S”¢H2SeČŪ·ŠµćÓɵĶµ½øßµÄĖ³Šņ£ŗ_________________”£
£Ø5£©HF±ČHClČČĪČ¶ØŠŌ____£ØĢī”°Ēæ”±»ņ”°Čõ”±£©£¬ŌŅņŹĒ£ŗ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬ŌŚ¹Ģ¶ØĢå»żµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ2HI(g)![]() H2(g)+I2(g)£¬0”«15sÄŚc(HI)ÓÉ0.lmol/L½µµ½0.07mol/L£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
H2(g)+I2(g)£¬0”«15sÄŚc(HI)ÓÉ0.lmol/L½µµ½0.07mol/L£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )
A. ČŻĘ÷ÖŠ£¬·“Ó¦Ę½ŗāŹ±µÄŃ¹Ēæ“óÓŚĘšŹ¼Ź±µÄŃ¹Ēæ
B. c(HI)ÓÉ0.07mol/L½µµ½0.05mol/LĖłŠčµÄ·“Ó¦Ź±¼ä“óÓŚ10s
C. ÉżøßĪĀ¶ČÕż·“Ó¦ĖŁĀŹ¼Óæģ£¬Äę·“Ó¦ĖŁĀŹ¼õĀż
D. 0”«15sÄŚÓĆI2±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ£ŗv(I2)=0.002mol/(L”¤s)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ŲÓŚŹµŃéŹŅÖʱøŅŅĻ©µÄŹµŃ飬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.·“Ó¦ĪļŹĒŅŅ“¼ŗĶ¹żĮæµÄ3mol/LĮņĖįµÄ»ģŗĻŅŗ
B.ĪĀ¶Č¼Ę²åČė·“Ó¦ŅŗĆęŅŌĻĀ£¬ŅŌ±ćæŲÖĘĪĀ¶ČŌŚ140”ę
C.·“ӦȯĘ÷£ØÉÕĘ棩֊Ӧ¼ÓČėÉŁŠķĖé“Éʬ
D.·“Ó¦Ķź±ĻĻČĻØĆš¾Ę¾«µĘŌŁ“ÓĖ®ÖŠČ”³öµ¼¹Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£ØĢāĪÄ£©ŗ¬Ģ¼ĪļÖŹŌŚČÕ³£Éś»īÓė¹¤ŅµÉś²śÉĻÓŠ¹ć·ŗµÄÓ¦ÓĆ”£
£Ø1£©Ņ»ÖÖČŪČŚĢ¼ĖįŃĪČ¼ĮĻµē³ŲŌĄķŹ¾ŅāČēĶ¼1ĖłŹ¾£¬Š“³öµē¼«AÖŠ·¢ÉśµÄµē¼«·½³ĢŹ½_____£»

£Ø2£©ĄūÓĆ¹āÄÜŗĶ¹ā“߻ƼĮ£¬æɽ«CO2ŗĶH2O(g)×Ŗ»ÆĪŖCH4ŗĶO2”£×ĻĶā¹āÕÕÉ䏱£¬ŌŚ²»Ķ¬“߻ƼĮ£ØI”¢¢ņ£¬¢ó£©×÷ÓĆĻĀ£¬CH4²śĮæĖę¹āÕÕŹ±¼äµÄ±ä»Æ¼ūĶ¼2”£ŌŚ15Š”Ź±ÄŚ£¬CH4µÄĘ½¾łÉś³ÉĖŁĀŹI”¢¢ņŗĶ¢ó“ӓ󵽊”µÄĖ³ŠņĪŖ______________£ØĢīŠņŗÅ£©”£

£Ø3£©ŅŌ TiO2/Cu2Al2O4ĪŖ“߻ƼĮ£¬æÉŅŌ½«CO2ŗĶCH4Ö±½Ó×Ŗ»Æ³ÉŅŅĖį”£ŌŚ²»Ķ¬ĪĀ¶ČĻĀ“߻ƼĮµÄ“߻Ɗ§ĀŹÓėŅŅĖįµÄÉś³ÉĖŁĀŹµÄ¹ŲĻµ¼ūĶ¼3”£ŅŅĖįµÄÉś³ÉĖŁĀŹÖ÷ŅŖČ”¾öÓŚĪĀ¶ČÓ°ĻģµÄ·¶Ī§ŹĒ______________________£»
£Ø4£©COŗĶH2ŌŚCu2O/ZnO×÷“߻ƼĮµÄĢõ¼žĻĀ·¢Éś·“Ó¦£ŗCO(g)+2H2(g)![]() CH3OH(g)»ńµĆ¼×“¼”£Ļņ2LµÄĆܱÕČŻĘ÷ÖŠĶØČė1mol CO(g)ŗĶ2mol H2(g)£¬·¢Éś·“Ó¦ŗĻ³É¼×“¼£¬·“Ó¦¹ż³ĢÖŠ£¬CH3OHµÄĪļÖŹµÄĮæ£Øn£©ÓėŹ±¼ä£Øt£©¼°ĪĀ¶ČµÄ¹ŲĻµČēĶ¼4ĖłŹ¾”£
CH3OH(g)»ńµĆ¼×“¼”£Ļņ2LµÄĆܱÕČŻĘ÷ÖŠĶØČė1mol CO(g)ŗĶ2mol H2(g)£¬·¢Éś·“Ó¦ŗĻ³É¼×“¼£¬·“Ó¦¹ż³ĢÖŠ£¬CH3OHµÄĪļÖŹµÄĮæ£Øn£©ÓėŹ±¼ä£Øt£©¼°ĪĀ¶ČµÄ¹ŲĻµČēĶ¼4ĖłŹ¾”£

¢Ł500”ęµÄ“Ė·“Ó¦µÄĘ½ŗā³£ŹżK=________________£»
¢Ś¾ŻŃŠ¾æ£¬·“Ó¦¹ż³ĢÖŠĘš“ß»Æ×÷ÓƵÄĪŖCu2O£¬·“Ó¦ĢåĻµÖŠŗ¬ÉŁĮæµÄCO2 ÓŠĄūÓŚĪ¬³ÖCu2OµÄĮæ²»±ä£¬ŌŅņŹĒ________________£ØÓĆ»Æѧ·½³ĢŹ½±ķŹ¾£©”£
¢ŪŌŚ500”ęŗćŃ¹Ģõ¼žĻĀ£¬ĒėŌŚĶ¼4ÖŠ»³ö·“Ó¦ĢåĻµÖŠn(CH3OH)Ėꏱ¼ät±ä»ÆµÄ×ÜĒ÷ŹĘĶ¼________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĶ¼Ź¾Óė¶ŌÓ¦µÄŠšŹö²»Ļą·ūŗĻµÄŹĒ£Ø £©

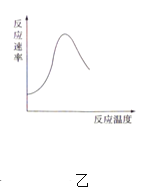


A. Ķ¼¼×±ķŹ¾Č¼ĮĻČ¼ÉÕ·“Ó¦µÄÄÜĮæ±ä»Æ
B. Ķ¼ŅŅ±ķŹ¾Ćø“߻Ʒ“Ó¦µÄ·“Ó¦ĖŁĀŹĖę·“Ó¦ĪĀ¶ČµÄ±ä»Æ
C. Ķ¼±ū±ķŹ¾³żČ„Ńõ»ÆĤµÄĆ¾ĢõĶ¶Čėµ½Ļ”ŃĪĖįÖŠ£¬·“Ó¦ĖŁĀŹvĖꏱ¼ätµÄ±ä»ÆĒśĻß
D. Ķ¼¶”±ķŹ¾Ä³ĪĀ¶ČĻĀV1mLl.0 mol/L HC1ČÜŅŗŗĶV2 mL1.5mol/LµÄNaOHČÜŅŗ»ģŗĻ¾łŌČŗóČÜŅŗĪĀ¶ČĖęV1µÄ±ä»ÆĒ÷ŹĘ(V1+V2=50mL)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆ¼Ūµē×Ó¶Ō»„³āĄķĀŪ£ØVSEPR£©æÉŅŌŌ¤²āŠķ¶ą·Ö×Ó»ņĄė×ÓµÄæռ乹ŠĶ£¬Ņ²æÉĶĘ²ā¼ü½Ē“󊔣¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ![]() ””””
””””![]()
A. CS2ŹĒVŠĪ·Ö×Ó B. SnBr2¼ü½Ē“óÓŚ![]()
C. BF3ŹĒČż½Ē׶ŠĪ·Ö×Ó D. NH4+¼ü½ĒµČÓŚ10928Ø@
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com