
【题目】在一真空容器中,充入10mol N2 , 30mol H2 , 发生反应N2(g)+3H2(g)2NH3(g),在一定条件下达到平衡时,N2的转化率为25%.若在同一容器中,在相同温度下,向容器中充入NH3 , 欲使达到平衡时各成分的质量分数与上述平衡相同,则起始时NH3的量和达到平衡时NH3的转化率为( )
A.20 mol、25%
B.20 mol、75%
C.40 mol、30%
D.10mol、50%
【答案】B
【解析】解:恒温恒容下,若开始只充入NH3 , 欲达到平衡时的各成份的百分含量与原平衡时相同,二者为等效平衡,由于反应前后气体的化学计量数之和不相等,故平衡时对应组分的物质的量相等,需要氨气的物质的量=10mol×2=20mol,原平衡中参加反应氮气为10mol×25%=2.5mol,由方程式可知平衡时氨气的物质的量=2.5mol×2=5mol,故若开始只充入NH3 , 氨气的转化率= ![]() ×100%=75%,
×100%=75%,
故选B.
【考点精析】解答此题的关键在于理解化学平衡的计算的相关知识,掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
A.氯碱工业,若X、Y均为石墨,Y附近能得到氯气
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C.外加电流的阴极保护法中,Y是待保护金属
D.电镀工业中,X是待镀金属,Y是镀层金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A、B、C三个装置的烧杯中分别盛有足量的CuCl2溶液.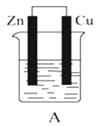
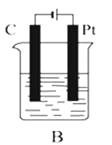
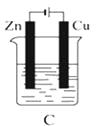
(1)A、B、C三个装置中属于原电池的是属于电解池的是 .
(2)A池中Zn是极,Cu极发生(填“氧化”或“还原”)反应,电极反应为 . 反应过程溶液中c(Cu2+)(填“变大”“变小”或“不变”).
(3)B池中C棒是极,一段时间后的现象为 , 电极反应为 . B 池中的总反应为 .
(4)C池在化学反应中发生的能量转化形式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一可逆反应2A(g)+3B(g)4C(g)+D(g),已知起始浓度c(A)=2mol/L,c(B)=3mol/L,c(C)=c(D)=0,反应开始20min后达到平衡状态,此时D的平衡浓度为0.5mol/L,则下列说法不正确的是( )
A.前20 min的平均反应速率v(C)=0.1 mol/(Lmin)
B.A的转化率为50%
C.C的平衡浓度c(C)=4 mol/L
D.B的平衡浓度c(B)=1.5 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对十二烷基苯磺酸钠 ![]() 是常用洗涤剂的主要成分.其结构可用图形
是常用洗涤剂的主要成分.其结构可用图形 ![]() 来表示,端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
来表示,端为链烃基,O端为极性基.根据这一结构特点,试分析和回答下列问题:
(1)Ⅰ.十二烷基苯磺酸钠分子在其水溶液表面分布的结构示意图应是下列各图中的图(填写序号),理由是 . 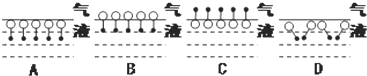
(2)进入介质(水)内部的十二烷基苯磺酸钠分子,可能会以下列结构形式中的存在(填写序号),理由是 . 
(3)Ⅱ.工业合成对十二烷基苯磺酸钠的一种路线如图所示: 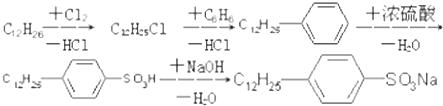
请回答下列问题:
产品中的亲油基是 .
(4)由十二烷基苯制取对十二烷基苯磺酸的化学方程式为 , 反应类型为 .
(5)在洗涤剂中添加酶制剂能促进污垢中的蛋白质(如奶渍、肉汤)等水解为可溶性的物质而被除去.使用加酶洗衣粉的水溶液中浸泡10~30min,水温在40~50℃最佳.加酶洗衣粉不宜在高温下、潮湿环境中贮存,也不宜久存.请解释原因 .
(6)过去使用的合成洗涤剂中常加入三聚磷酸钠(Na5P3O10)做助剂,它可使硬度大的洗涤水软化,对微细的无机粒子或油脂具有分散、乳化、胶溶作用,防止污渍再次沉积到衣物上;它还能维持水溶液的弱碱性,提高洗涤剂的去污能力和洗涤效果.但是,20世纪90年代以来,世界各国先后提出必须生产和使用无磷洗涤剂.请解释原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.主族元素的价电子全排布在最外层的ns或np轨道上
B.过渡元素的原子,价电子排布全部为(n-1)d1~10ns2
C.d轨道不可以参与化学键的形成
D.所有元素的共同特点是原子的价电子都排布在最外电子层上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表、元素周期律的说法正确的是
A. 稀有气体元素原子的最外层电子数均为8B. 元素周期表中有6个周期
C. 非金属性最强的元素是氟元素D. ⅠA族的元素全部是金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com