
| A. | 还原性F->Cl->S2- | B. | 原子半径:Na>Mg>O | ||
| C. | 酸性:H3PO4>H2SO4>HClO4 | D. | 乙烯比例模型  |
分析 A、非金属性越强,对应离子的还原性越弱;
B、电子层越多半径越大,电子层相同,核电荷越多半径越小;
C、非金属性越强,对应最高价氧化物的水化物的酸性越强;
D、 是乙烯球棍模型,而不是比例模型.
是乙烯球棍模型,而不是比例模型.
解答 解:A、非金属性越强,对应离子的还原性越弱,所以还原性F-<Cl-<S2-,故A错误;
B、电子层越多半径越大,电子层相同,核电荷越多半径越小,所以原子半径:Na>Mg>O,故B正确;
C、非金属性越强,对应最高价氧化物的水化物的酸性越强,非金属性:Cl>S>P,所以酸性为:H3PO4>H2SO4>HClO4,故C错误
D、 是乙烯球棍模型,而不是比例模型,故D错误;
是乙烯球棍模型,而不是比例模型,故D错误;
故选B.
点评 本题考查非金属元素的性质,明确同周期、同主族元素的性质变化规律及元素非金属性的比较方法是解答本题的关键,难度不大.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | C被还原 | B. | C发生氧化反应 | C. | ZnCO3被氧化 | D. | ZnCO3是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
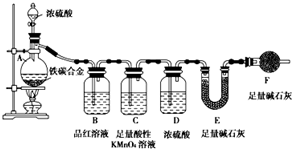 现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .请根据如图回答:
.请根据如图回答:
 .
. ;④
;④ .
. +C2H5OH
+C2H5OH查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电泳现象可证明胶体带电荷 | |
| B. | 胶体是一种纯净物 | |
| C. | 胶体属于介稳体系 | |
| D. | 将饱和氯化铁溶液滴入氢氧化钠溶液中制备氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
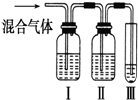 为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应.
为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先用乙醇和浓硫酸为原料制取乙烯,将生成的气体直接通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入试剂按①SO42- ②Cl- ③OH-的正确顺序可以将混合液中Cu2+、Ba2+、Ag+逐一沉淀出来加以分离 | |
| B. | 配制480mL 1.0mol•L-1的NaOH溶液时,用托盘天平称取19.2gNaOH固体 | |
| C. | 用萃取分液的方法除去酒精中的水 | |
| D. | 用可见光束照射以区别溶液和胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com