
在体积都为1L、pH都等于2的盐酸和醋酸溶液中,投入0.65g锌粒,则下列各图所示内容比较符合客观事实的是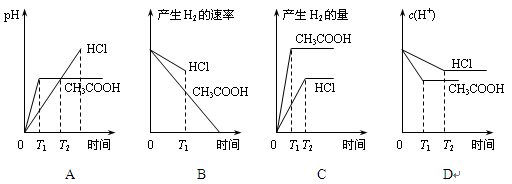
C
解析试题分析:体积相等,pH相等,说明盐酸浓度是0.01mol/L,醋酸浓度要大于0.01mol/L,加入的锌粒是0.01mol。
因为醋酸在反应过程中还不断电离,氢离子浓度减小的慢,所以pH升高的慢,斜率比盐酸的要小,A项错误;同理,产生氢气的速率取决于氢离子浓度,随着反应的进行,醋酸比盐酸中氢离子浓度大,反应速率快,B项错误;因为醋酸的物质的量比盐酸多,所以产生的氢气多,C项正确;醋酸中氢离子反应后又不断电离氢离子,所以浓度减小的比盐酸要慢,D错误。
考点:强弱电解质与金属反应产生氢气的速率及氢离子浓度的变化。
点评:对于弱电解质的电离,要注意随着氢离子浓度的减小,电离平衡向正向移动,氢离子的浓度降低的速率减缓。


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源:2013届黑龙江省高二上学期期末考试化学试卷 题型:选择题
在体积都为1L、pH都等于2的盐酸和醋酸溶液中,投入0.65g锌粒,则下列各图所示内容比较符合客观事实的是
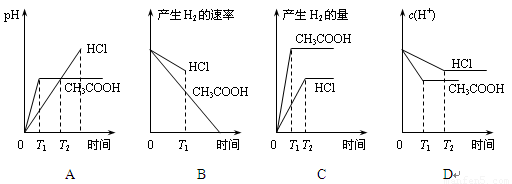
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com