
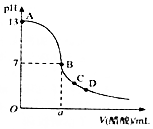
 298K时,在20mLbmol•L-1氧氧化钠溶液中滴入0.10mol•L-1的醋酸,溶液的pH与所加醋酸的体积关系如图所示.下列有关叙述正确的是( )
298K时,在20mLbmol•L-1氧氧化钠溶液中滴入0.10mol•L-1的醋酸,溶液的pH与所加醋酸的体积关系如图所示.下列有关叙述正确的是( )| A. | a<20 | |
| B. | C点溶液中:c(CH3COO-)+c(CH3COOH)=c(Na+) | |
| C. | A、B、C、D四点水的电离程度大小顺序为:D>B>C>A | |
| D. | 醋酸的电离平衡常数Ka=2.0×10-7/(0.la-2) |
分析 根据图象可知NaOH溶液的pH=13,则其浓度为0.1mol/L,
A.a=20时二者恰好反应才醋酸钠,溶液呈碱性,若为中性,则加入醋酸溶液体积大于20mL;
B.C点溶液的pH<7,呈酸性,则c(H+)>c(OH-),结合电荷守恒判断;
C.酸溶液的酸性(碱溶液的碱性)越强,水的电离程度越小,则B点水的电离程度最大;
D.B点时溶液的pH=7,c(H+)=c(OH-)=10-7mol/L、c(CH3COO-)=c(Na+)=$\frac{0.1mol/L×0.02L}{0.02L+0.00aL}$=$\frac{2}{20+a}$mol/L,根据物料守恒计算出醋酸的浓度,然后利用电离平衡常数的表达式计算.
解答 解:根据图象可知NaOH溶液的pH=13,则其浓度为0.1mol/L,
A.当a=20时,等体积、等浓度的氢氧化钠与醋酸恰好反应生成醋酸钠,溶液显示碱性,若为中性时,需要加入过量的醋酸,即a>20,故A错误;
B.C点时溶液的pH<7,则c(H+)>c(OH-),根据电荷守恒可知:c(CH3COO-)>c(Na+),则c(CH3COO-)+c(CH3COOH)>c(Na+),故B错误;
C.酸溶液和碱溶液都抑制了水的电离,A点溶液中氢氧根离子浓度最大,对水的电离抑制程度最大,则A点水的电离程度最小;C、D呈酸性,都抑制了水的电离,氢离子浓度越大,水的电离程度越小,则水的电离程度C>D,所以A、B、C、D四点水的电离程度大小顺序为:B>C>D>A,故C错误;
D.B点时溶液的pH=7,c(H+)=c(OH-)=10-7mol/L、c(CH3COO-)=c(Na+)=$\frac{0.1mol/L×0.02L}{0.02L+0.00aL}$=$\frac{2}{20+a}$mol/L,根据物料守恒可知:B点c(CH3COOH)=$\frac{0.1mol/L×0.00aL}{0.02L+0.00aL}$-$\frac{2}{20+a}$mol/L=$\frac{0.1a-2}{20+a}$mol/L,则该稳定性醋酸的电离平衡常数K=$\frac{1×1{0}^{-7}×\frac{2}{20+a}}{\frac{0.1a-2}{20+a}}$=$\frac{2×1{0}^{-7}}{0.1a-2}$,故D正确;
故选D.
点评 本题考查酸碱混合的定性判断及溶液pH的计算,题目难度中等,涉及离子浓度大小比较、电离平衡常数的计算、水的电离及其影响等知识,明确溶液酸碱性与溶液pH的关系为解答关键,试题有利于提高学生的分析、理解能力及综合应用能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯的实验式:C3H6 | B. | CO2的电子式: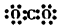 | ||
| C. | 镁离子的结构示意图: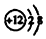 | D. | 中子数为18 的氯原子符号:1718Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮气是由氮原子构成的双原子分子,所以化学性质不活泼 | |
| B. | 1 mol N2可与3 mol H2完全反应生成2 mol NH3 | |
| C. | 电闪雷鸣的雨天,雨水中会含有一定量的硝酸,其中发生的反应之一是N2+2O2=2NO2 | |
| D. | NO、NO2在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C12与水反应:C12+H2O═2H++Cl-+ClO- | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | Fe跟HCl溶液反应:Fe+2H+═Fe2++H2↑ | |
| D. | BaCO3与盐酸反应:CO32-+2 H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 131I的质量数为131 | B. | 1mol 131I的质量为131 | ||
| C. | 131I原子核外有5个电子层 | D. | 131I核外最外层电子数为7e- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
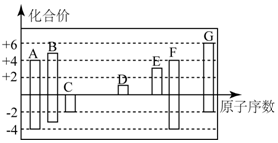 如图是部分短周期元素的常见化合价与原子序数的关系:
如图是部分短周期元素的常见化合价与原子序数的关系: ,其所含化学键类型为离子键和非极性键.
,其所含化学键类型为离子键和非极性键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高价氧化物对应水化物的碱性:乙>丙 | |
| B. | 简单气态氢化物的稳定性:丁>甲 | |
| C. | 简单离子半径:乙>丙>丁 | |
| D. | 甲和乙组成的化合物只存在离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com