
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
分析 根据反应可知A为酯类物质,而B为醇,根据质量守恒定律可求出B的分子式为C4H10O,由分子式C4H9OH看出属于一元醇,其同分异构体的数目等于丁基的数目,据此解题.
解答 解:根据反应可知A为酯类物质,而B为醇;根据质量守恒定律可求出B的分子式为C4H10O,由分子式C4H9OH看出属于一元醇,其同分异构体的数目等于丁基的数目,-C4H9有4种结构,分别为:CH3-CH2-CH2-CH2-、CH3-CH2-CH(CH3)-、(CH3)2CH-CH2-、(CH3)3C-,所以C4H10O的醇就有4种同分异构体.
故选A.
点评 本题考查同分异构体的判断,难度不大,做题时可以利用烃基异构判断,注意掌握同分异构体的概念及求算方法.


 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ③④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇分子结构中不存在手性碳 | |
| B. | 在NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | SO2、SO3都是极性分子 | |
| D. | 原子晶体中原子以共价键结合,具有键能大、硬度大的特性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
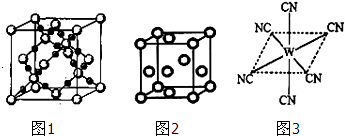
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
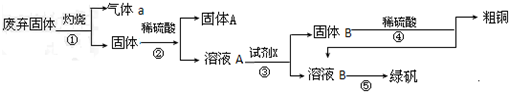
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com