
【题目】常温下,向20mL0.1mol L-1HB溶液中逐滴滴入 0.1mol L-1NaOH溶液,所得 PH变化曲线如图所示。下列说法错误的是

A.OA各点溶液均存在:c(B-) >c(Na+)
B.C至 D各点溶液导电能力依次增强
C.点 O时,pH>1
D.点 C时,X约为 10.4
【答案】D
【解析】
A.OA各点显酸性,则c(H+)>c(OH-),溶液中存在电荷守恒:c(H+)+c(Na+)= c(OH-)+c(B-),则c(B-)> c(Na+),A选项正确;
B.C至D各点溶液中,C点浓度为0.05mol·L-1,C之后加入的c(NaOH)为0.1mol·L-1,导电能力依次增强,B选项正确;
C.定性分析有:氢氧化钠溶液滴入20mL时达到终点,pH>7,HB为弱酸,O点pH>1,C选项正确;
D.C点为刚好反应完全的时候,此时物质c(NaB)=0.05mol·L-1,B-水解常数为Kh=10-14/(2×10-5)=5×10-10,B-水解生成的c(OH-)=![]() =5×10-6 mol·L-1,C点c(H+)=2×10-9 mol·L-1,C点pH=9-lg2=8.7,即x=8.7,D选项错误;
=5×10-6 mol·L-1,C点c(H+)=2×10-9 mol·L-1,C点pH=9-lg2=8.7,即x=8.7,D选项错误;


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】常温下,用NaOH溶液滴定H2C2O4溶液,溶液中-lg[c(H+)/c(H2C2O4)]和-lgc(HC2O4-)或-lg[c(H+)/c(HC2O4-)]和-lgc(C2O42-)关系如图所示,下列说法错误的是( )
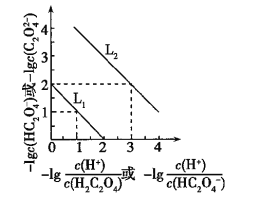
A. Ka1(H2C2O4)=1×10-2
B. 滴定过程中,当pH=5时,C(Na+)-3C(HC2O4-)>0
C. 向1 mol/L的H2C2O4溶液中加入等体积等浓度的NaOH溶液,完全反应后显酸性
D. 向0.1 mol/L的H2C2O4溶液中加水稀释,C(HC2O4-)/C(H2C2O4)比值将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:2SO2+O2![]() 2SO3(g),已知反应过程中某一时刻SO2、O2和SO3浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1。当反应达到平衡时,可能存在的数据是
2SO3(g),已知反应过程中某一时刻SO2、O2和SO3浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1。当反应达到平衡时,可能存在的数据是
A.SO2为0.4 mol·L-1、O2为0.2 mol·L-1B.SO2为0.3 mol·L-1
C.SO3为0.4 mol·L-1D.SO2、SO3均为0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列4种有机化合物
A:CH2=CH2 B:![]() C:CH3COOH D:
C:CH3COOH D: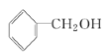
(1)写出化合物A、C中官能团的名称________、_______;
(2)4种化合物中能使溴的四氯化碳溶液褪色的是____(写名称);反应的化学方程为:_____;具有特殊气味、常做有机溶剂的是_____(写名称)。
(3)4种化合物中能与NaOH发生中和反应的是_____(写名称)。
(4)C与D在浓硫酸存在下,加热时生成的有机物的结构简式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的叙述中正确的是( )
A.在SiO2晶体中,由Si、O构成的最小单元环中共有8个原子
B.在28g晶体硅中,含Si﹣Si共价键个数为4NA
C.金刚石的熔沸点高于晶体硅,是因为C﹣C键键能小于Si﹣Si键
D.镁型和铜型金属晶体的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素a、b、c、d、e,原子序数依次增大,a是组成物质种类最多的元素,c是地壳中含量最多的元素,d与a同族,e2+离子3d轨道中有9个电子。回答下列问题:
(1)d原子的基态原子电子排布式为____________
(2)晶体d、晶体da、晶体ac2的熔点由高到低的顺序为__________ (用化学式表示,下同),a、b、c三种元素的第一电离能由大到小的顺序为________________________。
(3)元素b、c形成两种常见阴离子bc2-和bc3-,其中bc2-离子的中心原子杂化轨道类型为____________,bc3-离子的空间构型为____________。
(4)e单质的晶胞结构如图所示,e原子半径为rpm,e晶体密度的计算式为_________g·cm-3。(用含NA、r的表达式表示)
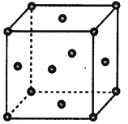
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请结合下方几种有机物的相互转化图回答:

(1)乙烯的电子式是______________________。
(2)反应①②的反应类型分别是__________、__________。
(3)Y的官能团名称是_____________________。
(4)X+Z→W的化学方程式是_________________________________,实验室常用下图 所示的装置实现这一转化。试管b中一般加入______________溶液,从试管b中分离出W的方法是_______。

(5)W的分子式__________,W属于羧酸类的同分异构体有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某有机物A的质量为9.0克,完全燃烧后生成13.2克二氧化碳和5.4克水,且此有机物的蒸气的相对密度是相同状况下氢气的45倍,取等量的该有机物分别与足量Na和NaHCO3溶液反应,生成的H2和CO2体积相等,求:
①此有机物的分子式为_________。
②2mol该有机物参与反应可生成1mol六元环的酯,写出该酯化反应方程式_________。
(2)某烃B的相对分子质量为84。回答下列问题:
①下列物质与B以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)_________。
a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
②若链烃B分子中所有的碳原子共平面,该分子的一氯取代物只有一种,则B与HCl发生加成反应的化学方程式_________。
③若烃B不能使溴水褪色,并且其一氯代物只有一种,则B的二氯代物的同分异构体有_________种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程不能达到实验目的的是( )
实验目的 | 实验过程 | |
A | 探究维生素C的还原性 | 向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
B | 配制100mL1.0mol/L CuSO4溶液 | 将25.0gCuSO4·5H2O配成100mL溶液 |
C | 验证X溶液中是否含有Fe2+ | 向X溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,观察溶液颜色变化 |
D | 除去固体KNO3中少量的NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤、洗涤、干燥 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com