
【题目】在一体积固定的密闭容器中加入反应物A,B,发生如下反应:A+2B3C.反应经2min后,A的浓度从开始时的1.0mol/L降到0.8mol/L.已知反应开始时B的浓度是0.8mol/L, 求:
(1)2min末B,C的浓度;
(2)2min内C的平均化学反应速率;
(3)2min末时物质B的转化率.
【答案】
(1)解:经2min后,A的浓度从开始时的1.0mol/L降到0.8mol/L.已知反应开始时B的浓度是0.8mol/L,则
A+ | 2B | 3C | ||
开始 | 1.0 | 0.8 | 0 | |
转化 | 0.2 | 0.4 | 0.6 | |
2min | 0.8 | 0.4 | 0.6 |
由上述分析可知,2min末B,C的浓度为0.6mol/L,
答:2min末B,C的浓度为0.6mol/L
(2)解:2min内C的平均化学反应速率为 ![]() =0.3mol/(L.min),
=0.3mol/(L.min),
答:2min内C的平均化学反应速率为0.3mol/(L.min)
(3)解:2min末时物质B的转化率为 ![]() ×100%=50%,
×100%=50%,
答:2min末时物质B的转化率为50%
【解析】经2min后,A的浓度从开始时的1.0mol/L降到0.8mol/L.已知反应开始时B的浓度是0.8mol/L,则
A+ | 2B | 3C | ||
开始 | 1.0 | 0.8 | 0 | |
转化 | 0.2 | 0.4 | 0.6 | |
2min | 0.8 | 0.4 | 0.6 |
并结合v= ![]() 、转化率=
、转化率= ![]() ×100%计算.
×100%计算.
【考点精析】解答此题的关键在于理解化学平衡的计算的相关知识,掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
【题目】某小组同学利用下图所示装置进行铁的电化学腐蚀原理的探究实验:
装置 | 分别进行的操作 | 现象 |
| i. 连好装置一段时间后,向烧杯中滴加酚酞 | |
ii. 连好装置一段时间后,向烧杯中滴加K3[Fe(CN)6]溶液 | 铁片表面产生蓝色沉淀 |
(1)小组同学认为以上两种检验方法,均能证明铁发生了吸氧腐蚀。
①实验i中的现象是______。
②用电极反应式解释实验i中的现象:______。
(2)查阅资料:K3[Fe(CN)6]具有氧化性。
①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是______。
②进行下列实验,在实验几分钟后的记录如下:
实验 | 滴管 | 试管 | 现象 |
| 0.5 mol·L-1 K3[Fe(CN)6]溶液 | iii. 蒸馏水 | 无明显变化 |
iv. 1.0 mol·L-1NaCl 溶液 | 铁片表面产生大量蓝色沉淀 | ||
v. 0.5 mol·L-1Na2SO4溶液 | 无明显变化 |
a. 以上实验表明:在有______存在条件下,K3[Fe(CN)6]溶液可以与铁片发生反应。
b. 为探究Cl-的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。此补充实验表明Cl-的作用是______。
(3)有同学认为上述实验仍不够严谨。为进一步探究K3[Fe(CN)6]的氧化性对实验ii结果的影响,又利用(2)中装置继续实验。其中能证实以上影响确实存在的是______(填字母序号)。
实验 | 试剂 | 现象 |
A | 酸洗后的铁片、K3[Fe(CN)6]溶液(已除O2) | 产生蓝色沉淀 |
B | 酸洗后的铁片、K3[Fe(CN)6]和NaCl混合溶液(未除O2) | 产生蓝色沉淀 |
C | 铁片、K3[Fe(CN)6]和NaCl混合溶液(已除O2) | 产生蓝色沉淀 |
D | 铁片、K3[Fe(CN)6]和盐酸混合溶液(已除O2) | 产生蓝色沉淀 |
(4)综合以上实验分析,利用实验ii中试剂能证实铁发生了电化学腐蚀的实验方案是:连好装置一段时间后,取铁片(负极)附近溶液于试管中,_____(回答相关操作、现象),则说明负极附近溶液中产生了Fe2+,即发生了电化学腐蚀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年年底,中国石油全部完成国V标准车用汽柴油质量升级,以减少空气污染。下列物质中,不会造成空气污染的是
A. NO B. CO2 C. SO2 D. 粉尘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.用酸性KMnO4溶液鉴别乙烯和乙炔
B.将铁屑、溴水、苯混合可制得溴苯
C.调查发现有些装饰程度较高的居室中,由装饰材料缓慢释放出来的化学污染物浓度过高,影响健康,这些污染物主要是甲酸和SO2等气体
D.将铜丝在酒精灯火焰上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
混合物 | 试剂 | 分离方法 | |
A | 苯(苯酚) | 溴水 | 过滤 |
B | 乙烷(乙烯) | 氢气 | 加热 |
C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
D | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香族化合物A的分子式为C8H10O,它的结构中有两个甲基(﹣CH3),且它遇FeCl3溶液可发生显色反应,这样的结构共有( )
A.4种
B.5种
C.6种
D.7种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄色固体聚合硫酸铁(SPFS)是一种重要的无机高分子絮凝剂,极易溶于水,作为工业和生活污水处理等领域具有重要的应用。SPFS可表示成Fex(OH)y(SO4)z=nH2O改为Fex(OH)y(SO4)z·nH2O。工业上常用的一种制备流程为:(绿矾化学式为FeSO4·7H2O)

在SPFS的多个质量指标中,盐基度是重要的质量指标之一,盐基度定义为:盐基度=n(OH-)/3n( Fe) ×100%。式中n(OH-)、n(Fe)分别表示固体聚合硫酸铁中OH一和Fe的物质的量。试回答下列问题。
(1)在绿矾中加入酸性介质的NaClO3目的是__________ 。
(2)实验室进行“蒸发”时用到的仪器有铁架台(带铁圈)、酒精灯和_______ 、______
(3)SPFS溶于水后并与水反应生成________ 能吸附水中的悬浮物来净化水。
(4)取15.05g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀20.97g.向上述滤液中加人NH3H2O,调节溶液pH= 6,经过滤、洗涤、干燥得Fe2O3固体5.60g。该固体聚合硫酸铁的盐基度为______ 。
(5)计算出该固体聚合硫酸铁样品的化学式(写出计算过程)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A. 10g46%的乙醇水溶液中所含氢原子数目为1.2NA
B. 1L1mol/L Na2CO3溶液中含有NA个CO32-
C. 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g
D. 常温下pH=1的H2SO4溶液中,H+的浓度为0.20mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
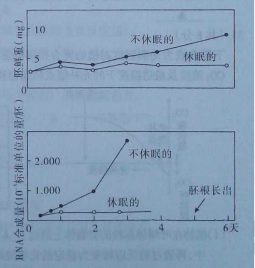
(1)通过不休眠种子与休眠种子胚的鲜重比较,得出其中结合水/自由水比值高的是_______种子;不休眠的种子萌发6天后至形成叶片前,干重会____________,原因是:____________。
(2)不休眠的种子萌发后胚中的RNA合成量____________,经分析种子的淀粉含量下降而葡萄糖含量升高,推测某些RNA控制翻译合成了______________。
(3)第5天萌发种子的胚根长出,此时整个种子内DNA的含量与不萌发种子比__________(相等、增多、减少),推测的理由是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com