
ijČÜŅŗÖŠŗ¬ÓŠµÄĄė×ÓæÉÄÜŹĒK+”¢Ba2+”¢A13+”¢Mg2+”¢AlO2£”¢CO32£”¢SiO32£”¢Cl£ÖŠµÄ¼øÖÖ£¬ĻÖ½ųŠŠČēĻĀŹµŃé£ŗ¢ŁČ”ÉŁĮæČÜŅŗ¼ÓĒāŃõ»ÆÄĘČÜŅŗ¹ż³ĢÖŠĪŽ³ĮµķÉś³É
¢ŚĮķȔɣĮæŌČÜŅŗ£¬ÖšµĪ¼ÓČė5 mL0.2 mol”¤L-1ŃĪĖį£¬·¢ÉśµÄĻÖĻóŹĒ£ŗæŖŹ¼²śÉś³Įµķ²¢Öš½„Ōö¶ą£¬³ĮµķĮæ»ł±¾²»±äŗó²śÉśĘųĢ壬×īŗó³ĮµķÖš½„¼õÉŁÖĮĻūŹ§”£
¢ŪŌŚÉĻŹö¢Ś³ĮµķĻūŹ§ŗóµÄČÜŅŗÖŠ£¬ŌŁ¼ÓČė×ćĮæµÄĻõĖįŅųČÜŅŗæɵƵ½³Įµķ0.43 g”£
ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£ŗ
A£®øĆČÜŅŗÖŠŅ»¶Ø²»ŗ¬Ba2+ ”¢Mg2+”¢A13+”¢SiO32£”¢Cl£
B£®øĆČÜŅŗÖŠŅ»¶Øŗ¬ÓŠK+”¢AlO2£”¢CO32£”¢Cl£
C£®øĆČÜŅŗŹĒ·ńÓŠK+ Šč×öŃęÉ«·“Ó¦£ØĶø¹żĄ¶É«īܲ£Į§Ę¬£©
D£®æÉÄÜŗ¬ÓŠCl£
B
”¾½āĪö”æ
ŹŌĢā½āĪö£ŗ¢ŁĻņČÜŅŗÖŠ¼ÓĒāŃõ»ÆÄĘČÜŅŗ¹ż³ĢÖŠĪŽ³ĮµķÉś³É£¬ĖµĆ÷ČÜŅŗÖŠŅ»¶Ø²»“ęŌŚÓėĒāŃõ»ÆÄĘÉś³É³ĮµķµÄĄė×Ó£ŗA13+”¢Mg2+£»¢ŚĻņŌČÜŅŗÖŠÖšµĪ¼ÓČė5mL0.2mol?L-1ŃĪĖį£¬æŖŹ¼²śÉś³Įµķ²¢Öš½„Ōö¶ą£¬³ĮµķĮæ»ł±¾²»±äŗó²śÉśĘųĢ壬×īŗó³ĮµķÖš½„¼õÉŁÖĮĻūŹ§£»µĪ¼ÓŃĪĖį²śÉśŗĶČܽāµÄ³ĮµķĪŖĒāŃõ»ÆĀĮ£¬ĘųĢåĪŖ¶žŃõ»ÆĢ¼£¬ĖµĆ÷ŌČÜŅŗÖŠ“ęŌŚAlO2-ŗĶCO32-£¬ĖłŅŌŅ»¶Ø²»“ęŌŚ²»ČÜÓŚŃĪĖįµÄSiO32-ŗĶÓėCO32-·“Ó¦µÄBa2+£¬ŌŁøł¾ŻČÜŅŗµēÖŠŠŌæÉÖŖ£ŗČÜŅŗÖŠŅ»¶Ø“ęŌŚĪØŅ»µÄŃōĄė×Ó£ŗK+£»¢ŪŌŚ¢Ś³ĮµķĻūŹ§ŗóµÄČÜŅŗÖŠ£¬ŌŁ¼ÓČė×ćĮæµÄĻõĖįŅųČÜŅŗæɵƵ½³Įµķ0.43g£¬³ĮµķĪŖAgCl£¬ĪļÖŹµÄĮæĪŖ£ŗ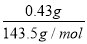 ”Ö0.003mol£»¢ŚÖŠ¼ÓČėµÄĀČĄė×ÓµÄĪļÖŹµÄĮæĪŖ£ŗn£ØHCl£©=0.2mol/L”Į0.005L=0.001mol£¼n£ØAgCl£©£¬ĖłŅŌŌČÜŅŗÖŠŅ»¶Ø“ęŌŚ0.02mol Cl-£¬A”¢øł¾ŻŅŌÉĻ·ÖĪöæÉÖŖ£¬ČÜŅŗÖŠŅ»¶Ø²»“ęŌŚBa2+”¢Mg2+”¢A13+”¢SiO32-£¬Ņ»¶Ø“ęŌŚCl-£¬¹ŹA“ķĪó£»B”¢ÓÉ·ÖĪöæÉÖŖ£ŗøĆČÜŅŗÖŠŅ»¶Øŗ¬ÓŠK+”¢AlO2-”¢CO32-”¢Cl-£¬¹ŹBÕżČ·£»C”¢øł¾ŻČÜŅŗµÄµēÖŠŠŌæÉŅŌÅŠ¶Ļ£¬ČÜŅŗÖŠŅ»¶Ø“ęŌŚ¼ŲĄė×Ó£¬²»ŠčŅŖĶعżŃęÉ«·“ӦŊ¶Ļ¼ŲĄė×ÓŹĒ·ń“ęŌŚ£¬¹ŹC“ķĪó£»D”¢øł¾ŻÉś³ÉĀČ»ÆŅų³ĮµķµÄĪļÖŹµÄĮææÉÖŖ£¬ŌČÜŅŗÖŠŅ»¶Ø“ęŌŚĀČĄė×Ó£¬¹ŹD“ķĪó”£
”Ö0.003mol£»¢ŚÖŠ¼ÓČėµÄĀČĄė×ÓµÄĪļÖŹµÄĮæĪŖ£ŗn£ØHCl£©=0.2mol/L”Į0.005L=0.001mol£¼n£ØAgCl£©£¬ĖłŅŌŌČÜŅŗÖŠŅ»¶Ø“ęŌŚ0.02mol Cl-£¬A”¢øł¾ŻŅŌÉĻ·ÖĪöæÉÖŖ£¬ČÜŅŗÖŠŅ»¶Ø²»“ęŌŚBa2+”¢Mg2+”¢A13+”¢SiO32-£¬Ņ»¶Ø“ęŌŚCl-£¬¹ŹA“ķĪó£»B”¢ÓÉ·ÖĪöæÉÖŖ£ŗøĆČÜŅŗÖŠŅ»¶Øŗ¬ÓŠK+”¢AlO2-”¢CO32-”¢Cl-£¬¹ŹBÕżČ·£»C”¢øł¾ŻČÜŅŗµÄµēÖŠŠŌæÉŅŌÅŠ¶Ļ£¬ČÜŅŗÖŠŅ»¶Ø“ęŌŚ¼ŲĄė×Ó£¬²»ŠčŅŖĶعżŃęÉ«·“ӦŊ¶Ļ¼ŲĄė×ÓŹĒ·ń“ęŌŚ£¬¹ŹC“ķĪó£»D”¢øł¾ŻÉś³ÉĀČ»ÆŅų³ĮµķµÄĪļÖŹµÄĮææÉÖŖ£¬ŌČÜŅŗÖŠŅ»¶Ø“ęŌŚĀČĄė×Ó£¬¹ŹD“ķĪó”£
æ¼µć£ŗĄė×ӵļģŃé



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ°²»ÕŹ”½ÄĻŹ®Š£øßČżÉĻѧʌʌĩĮŖæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
½ę×ÓĘų[(ClCH2CH2)2SŹĒŅ»ÖÖ¶¾Ęų£¬¼“Ź¹Šį¾õ²»ÄÜøŠŹÜµÄ¼«µĶÅضČŅ²»į¶ŌČĖŌģ³ÉÉĖŗ¦£¬æÉÓĆNaOHČÜŅŗ½ā¶¾”£½ę×ÓĘųæÉÓĆŅŌĻĀ·½·ØÖʱø 2CH2=CH2£«S2Cl2”ś(ClCH2CH2)2S£«SĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A£®½ę×ÓĘųŹĒÖ±ĻߊĶ·Ö×Ó B£®S2Cl2ÖŠÓŠ¼«ŠŌ¼üŗĶ·Ē¼«ŠŌ¼ü
C£®Öʱø·“Ó¦ÖŠS2Cl2£¬×÷»¹Ō¼Į D£®NaOHČÜŅŗ½ā¶¾ŌĄķŹĒÖŠŗĶ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÖŲĒģŹŠĘߊ£øßČżÉĻѧʌʌĩĮŖæ¼Ąķ×Ū»ÆѧŹŌ¾ķ £Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø¹²16·Ö£©
¢ń£®(10·Ö)ŅŃÖŖ2A(g)+B(g)  2C(g)£»”÷H=£a kJ£Æmol(a>0)£¬ŌŚŅ»øöÓŠ“߻ƼĮµÄ¹Ģ¶ØČŻ»żµÄČŻĘ÷ÖŠ¼ÓČė2molAŗĶ1molB£¬ŌŚ500”ꏱ³ä·Ö·“Ó¦“ļĘ½ŗāŗóCµÄÅضČĪŖw mol£ÆL,·Å³öČČĮæb kJ”£
2C(g)£»”÷H=£a kJ£Æmol(a>0)£¬ŌŚŅ»øöÓŠ“߻ƼĮµÄ¹Ģ¶ØČŻ»żµÄČŻĘ÷ÖŠ¼ÓČė2molAŗĶ1molB£¬ŌŚ500”ꏱ³ä·Ö·“Ó¦“ļĘ½ŗāŗóCµÄÅضČĪŖw mol£ÆL,·Å³öČČĮæb kJ”£
£Ø1£©±Č½Ļa b( Ģī > ”¢ = ”¢ < )
£Ø2£©ČōŌŚŌĄ“µÄČŻĘ÷ÖŠ£¬Ö»¼ÓČė2mol C£¬500”ꏱ³ä·Ö·“Ó¦“ļĘ½ŗāŗó£¬ĪüŹÕČČĮæckJ£¬CĪļÖŹµÄÅØ¶Č (Ģī>”¢=”¢<)w mol/L£¬a”¢b”¢cÖ®¼äĀś×ćµÄ¹ŲĻµŹ½ĪŖ (ÓĆŗ¬a”¢b”¢cµÄ“śŹżŹ½±ķŹ¾)”£
£Ø3£©ÄÜĖµĆ÷øĆ·“Ó¦ŅŃ¾“ļµ½Ę½ŗāדĢ¬µÄŹĒ ”£
a”¢V(C)=2V(B)£» b”¢ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
c”¢VÄę(A)=2VÕż(B) d”¢ČŻĘ÷ÄŚµÄĆܶȱ£³Ö²»±ä
£Ø4£©Čō½«ÉĻŹöČŻĘ÷øÄĪŖŗćŃ¹ČŻĘ÷(·“Ó¦Ē°Ģå»żĻąĶ¬)£¬ĘšŹ¼Ź±¼ÓČė2molAŗĶlmolB£¬500”ꏱ³ä·Ö·“Ó¦“ļĘ½ŗāŗ󣬷ųöČČĮæd kJ£¬Ōņd b ( Ģī > ”¢ = ”¢ < )£¬
¢ņ.£Ø6·Ö£©ÓĆĪüŹÕH2ŗóµÄĻ”ĶĮ“¢ĒāŗĻ½š×÷ĪŖµē³Ųøŗ¼«²ÄĮĻ£ØÓĆMH±ķŹ¾£©£¬
NiO£ØOH£©×÷ĪŖµē³ŲÕż¼«²ÄĮĻ£¬KOHČÜŅŗ×÷ĪŖµē½āÖŹČÜŅŗ£¬æÉÖʵĆøßČŻĮ棬³¤ŹŁĆüµÄÄųĒāµē³Ų”£µē³Ų³ä·ÅµēŹ±µÄ×Ü·“Ó¦ĪŖ£ŗ
NiO(OH)£«MH Ni(OH)2£«M
Ni(OH)2£«M
£Ø1£©µē³Ų·ÅµēŹ±£¬øŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ_______
£Ø2£©³äµēĶź³ÉŹ±£¬Ni£ØOH£©2Č«²æ×Ŗ»ÆĪŖNiO£ØOH£©”£Čō¼ĢŠų³äµē½«ŌŚŅ»øöµē¼«²śÉśO2£¬O2Ą©É¢µ½ĮķŅ»øöµē¼«·¢Éśµē¼«·“Ó¦±»ĻūŗÄ£¬“Ó¶ų±ÜĆā²śÉśµÄĘųĢåŅżĘšµē³Ų±¬ÕØ£¬“ĖŹ±£¬Ņõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”Š×÷ĢåøßČżÉĻѧʌµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĀČĖįŹĒŅ»ÖÖĒæĖį£¬ÅØ¶Č³¬¹ż40£„Ź±»į·¢Éś·Ö½ā£¬·“Ó¦æɱķŹ¾ĪŖ£ŗa HClO3 = bO2”ü+ cCl2”ü+ dHClO4 + eH2OÓĆŹŖČóµÄµķ·Ūµā»Æ¼ŲŹŌÖ½¼ģŃéĘųĢå²śĪļŹ±£¬ŹŌÖ½Ļȱ䥶ŗóĶŹÉ«”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ÓÉ·“Ó¦æÉČ·¶Ø£ŗŃõ»ÆŠŌHClO4£¾HClO3
B£®Čō»Æѧ¼ĘĮæŹża=8£¬b=3£¬ŌņøĆ·“Ó¦×ŖŅʵē×ÓŹżĪŖ20e£
C£®±äĄ¶µÄµķ·Ūµā»Æ¼ŲŹŌÖ½ĶŹÉ«ŹĒŅņĪŖæÉÄÜ·¢ÉśĮĖ£ŗ4C12 + I2 + 6H2O = 12H+ + 8Cl£+ 2IO3£
D£®ČōĀČĖį·Ö½āĖłµĆ»ģŗĻĘųĢ壬lmol»ģŗĻĘųĢåÖŹĮæĪŖ47.6g£¬Ōņ·“Ó¦·½³ĢŹ½æɱķŹ¾ĪŖ£ŗ26HClO3 = 15O2”ü+ 8C12”ü+ 10HClO4 + 8H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”Äž²ØŹŠøßČżŅ»ŌĀ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø12·Ö£©
£Ø1£©20”ꏱ0.1 mol”¤L£1NaOH·Ö±šµĪ¶Ø0.1 mol”¤L£1HCl”¢0.1 mol”¤L£1CH3COOHµÄpH±ä»ÆĒśĻßČēĻĀ”£
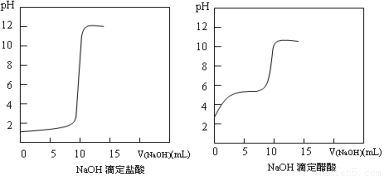
øł¾ŻÉĻŹöĒśĻß»Ų“šĻĀĮŠĪŹĢā£ŗ
¢Ł²āµĆ“×ĖįĘšµćpHĪŖ3£¬Ōņ20”ꏱøĆÅØ¶Č“×ĖįµÄµēĄė¶ČĪŖ £»
¢ŚµĪ¶ØæŖŹ¼ŗó“×ĖįĒśĻß±ä»Æ±ČŃĪĖįæģµÄŌŅņŹĒ £»
£Ø2£©25 ”ꏱ0.1 mol”¤L-1µÄH2RĖ®ČÜŅŗÖŠ£¬ÓĆĒāŃõ»ÆÄĘĄ“µ÷½ŚČÜŅŗpH£¬µĆµ½ŗ¬ÓŠH2R”¢HR£”¢R2£ČżÖÖĪ¢Į£µÄČÜŅŗ”£µ±c(Na+)=c(R2£)+c(HR£)+c(H2R)Ź±ČÜŅŗµÄČÜÖŹĪŖ (Ģī»ÆѧŹ½)”£
£Ø3£©ĻĀĶ¼ŹĒijĖ®ČÜŅŗŌŚpH“Ó0ÖĮ14µÄ·¶Ī§ÄŚH2CO3”¢HCO3£”¢CO32£ČżÖֳɷÖĘ½ŗāŹ±µÄ×é³É·ÖŹż”£
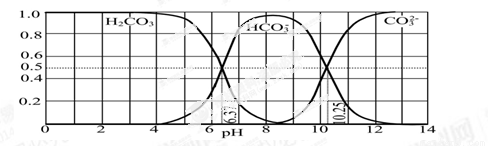
¢ŁĻĀĮŠŠšŹöÕżČ·µÄŹĒ ”£
A£®“ĖĶ¼ŹĒ1.0 mol”¤L£1Ģ¼ĖįÄĘČÜŅŗµĪ¶Ø1.0 mol”¤L£1 HClČÜŅŗµÄµĪ¶ØĒśĻß
B£®ŌŚpH·Ö±šĪŖ6.37¼°10.25Ź±£¬ČÜŅŗÖŠc(H2CO3)=c(HCO3£)=c(CO32£)
C£®ČĖĢåŃŖŅŗµÄpHŌ¼ĪŖ7.4£¬ŌņCO2ŌŚŃŖŅŗÖŠ¶ąŅŌHCO3£ŠĪŹ½“ęŌŚ
D£®ČōÓĆCO2ŗĶNaOH·“Ó¦ÖĘČ”NaHCO3£¬ŅĖæŲÖĘČÜŅŗµÄpHĪŖ7”«9Ö®¼ä
£Ø4£©½«ÄņĖŲŹ©ČėĶĮČĄŗ󣬓ó²æ·ÖŹĒĶعż×Ŗ»ÆĪŖĢ¼Ėįļ§»ņĢ¼ĖįĒāļ§ŗó²Å±»×÷ĪļĖłĄūÓĆ£¬ÄņĖŲ·Ö×ÓŌŚĪ¢ÉśĪļ·ÖĆŚµÄėåĆø×÷ÓĆĻĀ£¬×Ŗ»ÆĪŖĢ¼Ėįļ§”£ŅŃÖŖČõµē½āÖŹŌŚĖ®ÖŠµÄµēĄėĘ½ŗā³£Źż£Ø25”ę£©ČēĻĀ±ķ£ŗ
Čõµē½āÖŹ | H2CO3 | NH3”¤H2O |
µēĄėĘ½ŗā³£Źż | Ka1£½4.30”Į10-7 Ka2£½5.61”Į10-11 | 1.77”Į10-5 |
ĻÖÓŠ³£ĪĀĻĀ0.1 mol”¤L-1µÄ(NH4)2CO3ČÜŅŗ£¬
¢ŁÄćČĻĪŖøĆČÜŅŗ³Ź ŠŌ£ØĢī”°Ėį”±”¢”°ÖŠ”±”¢”°¼ī”±£©£¬ŌŅņŹĒ ”£
¢Ś¾ĶøĆČÜŅŗÖŠĮ£×ÓÖ®¼äÓŠĻĀĮŠ¹ŲĻµŹ½£¬ÄćČĻĪŖĘäÖŠÕżČ·µÄŹĒ ”£
A£®c (NH4+)£¾c (CO32-)£¾c (HCO3-)£¾c (NH3”¤H2O)
B£®c(NH4+)+c(H+)£½c(HCO3-)+c(OH-)+c(CO32-)
C£®c (CO32-) + c (HCO3-) +c (H2CO3)£½0.1 mol”¤L-1
D£®c (NH4+)+ c (NH3”¤H2O)£½2 c (CO32-) + 2c (HCO3-) +2 c (H2CO3)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”Äž²ØŹŠøßČżŅ»ŌĀ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢W”¢QŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĻĀ±ķĖłŹ¾£¬ĘäÖŠXŌŖĖŲµÄŌ×ÓÄŚ²ćµē×ÓŹżŹĒ×īĶā²ćµē×ÓŹżµÄŅ»°ė£¬ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
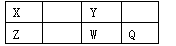
A£®WµĆµē×ÓÄÜĮ¦±ČQĒæ
B£®ÓÉZÓėY×é³ÉµÄĪļÖŹŌŚČŪČŚŹ±Äܵ¼µē
C£®ÄĘÓėYæÉÄÜŠĪ³ÉNa2Y 2»ÆŗĻĪļĒŅøĆ»ÆŗĻĪļĄė×Ó¼üŗĶ¹²¼Ū¼ü
D£®XÓŠ¶ąÖÖĶ¬ĖŲŅģŠĪĢ壬¶ųY²»“ęŌŚĶ¬ĖŲŅģŠĪĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”Äž²ØŹŠøßČżŅ»ŌĀ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÖŠ£¬ÕżČ·µÄŹĒ
A£®Na2OŗĶNa2O2×é³ÉŌŖĖŲĻąĶ¬£¬ĒŅ¶¼ÄÜÓėĮņĖįČÜŅŗ·“Ó¦
B£®¹āµ¼ĻĖĪ¬ÓÉSiO2ÖʱøµĆµ½£¬ĘäŹōÓŚ¹čĖįŃĪ²śĘ·
C£®¹¤ŅµÉĻĄūÓƵē½āČŪČŚµÄMgOĄ“ÖʱøĆ¾
D£®SO2ĶØČėŠĀÖĘĀČĖ®ÖŠ£¬ĀČĖ®ĶŹÉ«ŹĒŅņĪŖSO2¾ßÓŠĘư׊Ō
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÕć½Ź”ŗ¼ÖŻµŲĒų7Š£øßČżÉĻŃ§ĘŚĘŚÄ©Ä£ÄāĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĶ¼Ź¾Óė¶ŌÓ¦µÄŠšŹöĻą·ūµÄŹĒ

A£®Ķ¼¼×±ķŹ¾ĻņCH3COOHČÜŅŗÖŠÖš²½¼ÓČėCH3COONa¹ĢĢåŗó£¬ČÜŅŗpHµÄ±ä»Æ
B£®Ķ¼ŅŅ±ķŹ¾Ļņ“×ĖįČÜŅŗÖŠ¼ÓĖ®Ź±Ęäµ¼µēŠŌ±ä»Æ£¬ŌņCH3COOHČÜŅŗµÄpH£ŗa£¾b
C£®Ķ¼±ū±ķŹ¾“߻ƼĮÄÜøıä»Æѧ·“Ó¦µÄģŹ±ä
D£®Ķ¼¶”±ķŹ¾µČĮæNO2ŌŚČŻ»żĻąĶ¬µÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬²»Ķ¬ĪĀ¶ČĻĀ·Ö±š·¢Éś·“Ó¦£ŗ2NO2 (g) N2O4(g)£¬ĻąĶ¬Ź±¼äŗó²āµĆNO2ŗ¬ĮæµÄĒśĻߣ¬ŌņøĆ·“Ó¦µÄ”÷H£¼0
N2O4(g)£¬ĻąĶ¬Ź±¼äŗó²āµĆNO2ŗ¬ĮæµÄĒśĻߣ¬ŌņøĆ·“Ó¦µÄ”÷H£¼0
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğŗž±±Ź”ĻåŃōŹŠøßČż1ŌĀµ÷ŃŠĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ņ»¶ØĢõ¼žĻĀ£¬ČÜŅŗµÄĖį¼īŠŌ¶ŌTiO2¹ā“ß»ÆČ¾ĮĻR½µ½ā·“Ó¦µÄÓ°ĻģČēĶ¼ĖłŹ¾”£

ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
A£®ŌŚ0”«50 minÖ®¼ä£¬pH£½2ŗĶpH£½7Ź±RµÄ½µ½ā°Ł·ÖĀŹĻąµČ
B£®ČÜŅŗĖįŠŌŌ½Ē棬RµÄ½µ½āĖŁĀŹŌ½Š”
C£®RµÄĘšŹ¼ÅضČŌ½Š”£¬½µ½āĖŁĀŹŌ½“ó
D£®ŌŚ20”«25 minÖ®¼ä£¬pH£½10Ź±RµÄĘ½¾ł½µ½āĖŁĀŹĪŖ0.04 mol”¤L£1”¤min£1
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com