
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 物质的量是度量物质所含微观粒子多少的物理量 | |
| C. | 利用丁达尔效应可以区别溶液与胶体 | |
| D. | 等质量的O2和O3中所含氧原子个数相同 |
分析 A、物质的量的含义可知1mol任何物质都含有约6.02×1023个该物质的微粒;
B、物质的量是度量物质所含微观粒子多少的物理量;
C、胶体具有丁达尔效应,是胶体特有的性质,溶液不具有丁达尔效应;
D、O2和O3都是氧原子构成.
解答 解:A、物质的量的含义可知1mol任何物质都含有约6.02×1023个该物质的微粒,而不一定是原子,故A错误;
B、物质的量是科学上用来表示物质所含微观粒子多少的物理量,可用于表示一定数目粒子的集合体,故B正确;
C、光线透过胶体时,胶体中可发生丁达尔效应,丁达尔效应是胶体特有的性质,溶液不具有丁达尔效应,利用丁达尔效应可以区别溶液与胶体,故C正确;
D、O2和O3都是氧原子构成,等质量的O2和O3,也就是氧原子的质量相等,故D正确;
故选A.
点评 本题考查了物质的量的相关概念的理解和胶体性质,解题时须仔细审题,对照性质解答.题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 10 mL | B. | 5 mL | C. | 大于5mL | D. | 小于5mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| B. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| C. | 用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=5的NaHSO3溶液中:c(HSO3-)>c(SO${\;}_{3}^{2-}$)>c(H2SO3) | |
| B. | 使酚酞呈红色的苯酚与苯酚钠混合溶液中:c(Na+)>c(C6H5O-)>c(OH-)>c(H+) | |
| C. | 在0.1 mol•L-1 Na2CO3溶液中:c(HCO${\;}_{3}^{-}$)=c(H2CO3)+c(H+)-c(OH-) | |
| D. | 等物质的量浓度、等体积的NaOH溶液与CH3COOH溶液混合所得溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 地下钢管连接镁块 | B. | 金属护栏表面涂漆 | ||
| C. | 汽车底盘喷涂高分子膜 | D. | 水中的钢闸门连接电源的负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.0g C2H6中含有共用电子对的数目为0.7×6.02×1023 | |
| B. | 25℃时pH=1的醋酸溶液中含有H+的数目为0.1×6.02×1023 | |
| C. | 已知2CO(g)+O2(g)?2CO2(g)△H=-a kg•mol-1,将2NA个CO与NA个O2混合,充分反应放出a kJ的热量 | |
| D. | 50mL 18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(CH3COOH)>c(Na+) | B. | c(Na+)+c(H+)=c(OH-)+c(CH3COO-) | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(CH3COOH)=c(CH3COO-)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
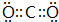 ,B与D形成的原子个数比为1:1的化合物的电子式是
,B与D形成的原子个数比为1:1的化合物的电子式是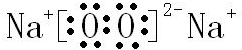 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com