
����Ŀ���±���Ԫ�����ڱ���һ���֣��������е���ĸ�ֱ����һ�ֻ�ѧԪ�ء�

�Իش��������⣺
(1)��д��Ԫ��M�Ļ�̬ԭ�ӵļ۵����Ų�ʽ��________________________��
(2)��״���£�11.2L AC2������������ĿΪ______��д��AC2�ĵ���ʽ��_________________��
(3)E��F��G�ĵ�һ�������ɴ�С��˳��Ϊ��____________������Ԫ�ط��ţ�
(4)LC2I2������Ϊ���ɫҺ�壬���� CCl4��CS2 �Ȼ��ܣ��ݴ˿��ж� LC2I2��________(���������������Ǽ�����)���ӡ�
(5)�ڢٱ�����CH3OH����CS2����C2H4����CCl4���������У�̼ԭ�Ӳ�ȡsp2�ӻ��ķ�����________(�����)��
(6)Ԫ��N�����γɷ���ʽΪCo��NH3��5BrSO4����λ����Ϊ6������������������һ����������Һ�м���BaCl2��Һʱ������������������AgNO3��Һʱ����������ɫ��������������Ļ�ѧʽΪ_______________��
���𰸡� ![]() 3d64s2 NA Mg��Al��Na �Ǽ��� �٢� [Co��NH3��5SO4]Br
3d64s2 NA Mg��Al��Na �Ǽ��� �٢� [Co��NH3��5SO4]Br
��������������Ҫ������ӽṹ��A��B��C��D��E��F��G��H��I��L��M��N�ֱ���̼���������������ơ�þ���������ȡ����������ܡ�
(1)Ԫ��M�Ļ�̬ԭ�ӵļ۵����Ų�ʽ��3d64s2��
(2)CO2���Ӻ��������м�����״���£�11.2L��0.5molAC2������������ĿΪNA��AC2�ĵ���ʽ��![]() ��
��
(3)һ�������Խǿ����һ������ԽС�������ԣ�Na>Mg>Al������Mgԭ���������Ӵ���ȫ�����Ľ��ȶ�״̬��ʹ��Mg�ĵ�һ�����ܴ�����������E��F��G�ĵ�һ�������ɴ�С��˳��Ϊ��Mg��Al��Na��
(4)LC2I2������Ϊ���ɫҺ�壬���� CCl4��CS2 �Ȼ��ܣ����ݡ��������ܡ����ж�LC2I2�ǷǼ��Է��ӡ�
(5)�ڢٱ�����CH3OH����CS2����C2H4����CCl4���������У�̼ԭ���ӻ���ʽ�ֱ��Ǣ�sp2����sp3����sp����sp2����sp3��̼ԭ�Ӳ�ȡsp2�ӻ��ķ����Т٢���
(6)Ԫ��N�����γɷ���ʽΪCo��NH3��5BrSO4����λ����Ϊ6������������������һ����������Һ�м���BaCl2��Һʱ������������˵��SO42-��Ϊ��λ������ڽ磬������AgNO3��Һʱ����������ɫ������˵��Br-����磬��������Ļ�ѧʽΪ[Co��NH3��5SO4]Br��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����٪�����У���������������٪�������͵�ʳ����������1.6����ǰ��٪�͡����й��������ڵĻ�ѧԪ���������ڵĻ�ѧԪ�ص�˵���У�����ܲ���ȷ����( )
A. ������ͬ B. ���ͬ
C. ����ͳһ�� D. ���в�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��л���ն��Σ�Cu2SO3��CuSO3��2H2O)��һ�ֲ�����ˮ������Ҵ��Ĺ��壬100��ʱ�����ֽ⡣����CuSO4��5H2O��SO2��Ϊԭ���Ʊ���ʵ��װ�D����ͼ��ʾ��
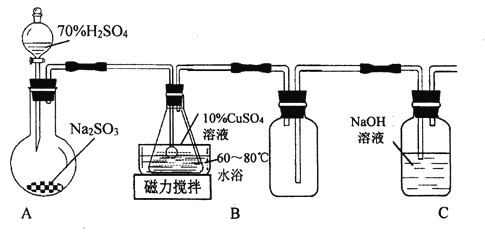
(1)װ��A�ڳ�������ȡSO2ʱ����70%���������ϡ�����98%Ũ���ᣬ��ԭ����________��
(2)װ��B�з�����Ӧ�����ӷ���ʽΪ_________��
(3)װ��C��������__________��
(4)��B�л�õĹ�������������ˮ���ϴ�ӣ�����ո�����鼺ϴ����ȫ�ķ�����________________��
(5)�벹�������ɹ�ҵ������ͭ��������FeO)�Ʊ�ʵ��ԭ�ϣ�����CuSO4��5H2O) ��ʵ�鷽������ҵ������ͭ�б߽�������Թ�����������Һ����ʹ����ȫ�ܽ⣬�߽���������е���______��Һ�������������________����3.2<pH<4.2�����ã����ˣ�����Һˮԡ��������Ũ����������־�Ĥ����ȴ�ᾧ�����ˣ���95% �ƾ�ϴ�Ӿ���2��3�Σ����ɣ��õ�CuSO4��5H2O��
[��֪������Һ���������↑ʼ�����������ȫʱ��pH��Χ�ֱ�Ϊ��Fe(OH)2 (5.8, 8.8); Cu(OH)2 (4.2, 6.7); Fe(OH)3 (1.1��3.2)]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.���ˮ�еμ�FeCl3��Һ�Ʊ�Fe��OH��3���壺Fe3++3H2O ![]() Fe��OH��3��+3H+
Fe��OH��3��+3H+
B.��С�մ�����θ����ࣺNaHCO3��+H+=Na++CO2��+H2O
C.ʵ������Ũ������MnO2��Ӧ��Cl2��MnO2+4H++2Cl�� ![]() Cl2��+Mn2++2H2O
Cl2��+Mn2++2H2O
D.��FeCl3��Һ��ʴӡˢ��·�壺Fe3++Cu=Fe2++Cu2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ν���ع������Ǵ�һЩ���ꡢ�Ƶ����ˮ�����̳����IJ���ʣ�������������ˮ�����Լ���������ӹ�����ʳ���������������̣�����ȥ�����е��������ʣ�������˫��ˮ����Ư�ף������빤ҵ���ݼ����ں�Ǧ�����Ԫ�ؼ��������ӻ��Ȼ���������������ƣ�����װ�ɳ�Ʒ�ͳ��۵������Ļ���ꡢ���ꡢ������ѧУ�����������ж���ȷ���ǣ� ��
A�����ع������������ͨʳ����һ�����������ϴ��������ع��������й̶����۷е�
B�����ع�����������������ԭ�ϣ������������Ȳ�Ʒ
C�����ع������ڼ������ݼ������������彡����Ӱ��
D�����ع���������Ҫ�ɷ��ǵ����ʣ������н϶���Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڷ�Ӧ��C+CO2��2CO�У���ʹ��Ӧ��������Ĵ�ʩ�� ( )
������ѹǿ �������¶� ��ͨ��CO2 ������̼���� �ݽ���ѹǿ
A���٢ڢ� B���ڢۢܢ� C���٢ڢۢ� D���ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1mol�Ҵ�(���е�����18O���)��Ũ������ڲ������������������ַ�Ӧ������������ȷ����( )
A.ˮ�����к���18OB.���������к���18O
C.������ϵ�����ַ����ж�����18OD.����90g��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ�У���ȷ����
A.FeƬͶ��Ũ�����У�Fe+2H+�� Fe2++H2��
B.��������Һ��������ռ���Һ�У�Al3++4OH���� AlO2��+ 2H2O
C.FeS����ϡ������Һ�У�S2��+2H+ ��H2S��
D.��AlCl3��Һ�м��������ˮ��Al3++4NH3��H2O�� AlO2��+4NH4++2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��20�ְ������ƽ����Է�������Ϊ128��������һ�����Ļ������10�������ṹ��һ����������ô�ö��ĵ���Է������������ٺ��еİ�����Ŀ�ֱ��� (����)
A. 1 280,11 B. 1 262,1 C. 1 118,1 D. 1 100,9
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com