
分析 原电池中,活泼性较强的电极为负极,活泼性较弱的电极为正极,放电时,电流从正极沿导线流向负极,正极上得电子发生还原反应,据此分析解答.
解答 解:原电池中,活泼性较强的电极为负极,活泼性较弱的电极为正极,放电时,电流从正极沿导线流向负极,正极上得电子发生还原反应,a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池,若a、b相连时,a为负极,则活泼性a>b;
c、d相连时,电流由d到c,则活泼性c>d;
a、c相连时,a极发生氧化反应,则活泼性a>c;
b、d相连时,b上有大量气泡产生,则活泼性d>b,
通过以上分析知,金属活泼性强弱顺序是a>c>d>b,
故答案为:a>c>d>b.
点评 本题以原电池原理为载体考查金属活泼性强弱判断,明确原电池正负极与金属活泼性的关系是解本题关键,再结合正负极的判断方法分析解答,题目难度不大.


科目:高中化学 来源: 题型:实验题
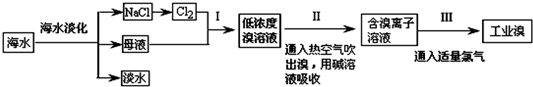
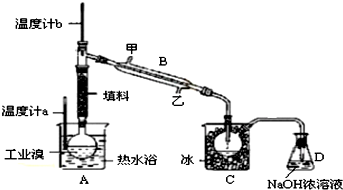
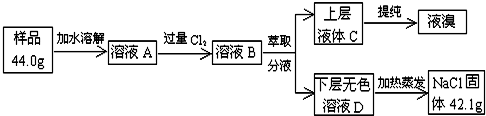
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电极B为正极,CO2在正极发生还原反应 | |
| B. | 电极A上H2参与的电极反应为:H2+CO32--2e-=CO2↑+H2O | |
| C. | 电极B上发生的电极反应为:4H++O2+4e-=2H2O | |
| D. | 电池工作时,CO32-向电极B移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝粉与氧化铁的反应 | B. | 炽热的炭与二氧化碳的反应 | ||
| C. | 锌片与稀硫酸反应 | D. | 氢氧化钠与盐酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有效地利用现有新能源和开发新能源已受到各国的重视.
有效地利用现有新能源和开发新能源已受到各国的重视.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1s电子云呈球形,表示电子绕原子核做圆周运动 | |
| B. | 电子云图中的小黑点密度大,说明该原子核外空间电子数目多 | |
| C. | 光谱分析可用于鉴定元素 | |
| D. | 3d3表示3d能级有3个轨道 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱属于碱 | B. | 小苏打不属于电解质 | ||
| C. | 水玻璃属于纯净物 | D. | CO不属于酸性氧化物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com