
| A�� | ƽ��ʱ����������ѹǿ����=��=�� | B�� | ƽ��ʱ��I2��Ũ�ȣ��ڣ���=�� | ||
| C�� | ƽ��ʱ��I2�������������=��=�� | D�� | �ӷ�Ӧ��ʼ����ƽ���ʱ�䣺�٣���=�� |
���� ���ݵ�Чƽ��ԭ������1mol H2��1molI2��ȫת��ΪHI����HIΪ2mol�����Ԣٺ͢�����ȫ��ͬ�ĵ�Чƽ�⣬���Զ��ߵ�Ũ�ȣ��ٷֺ�����ѹǿ��ת���ʵȶ�һ������������������HI�������÷�ӦΪ��Ӧǰ�������������ķ�Ӧ������HI�������ﵽƽ��ʱ��ƽ����ԭƽ����ͬ�����Ը����ʵİٷֺ������䣬����Ũ������
��� �⣺���ݵ�Чƽ��ԭ������1mol H2��1molI2��ȫת��ΪHI����HIΪ2mol�����Ԣٺ͢�����ȫ��ͬ�ĵ�Чƽ�⣬���Զ��ߵ�Ũ�ȣ��ٷֺ�����ѹǿת�����ʵȶ�һ������������������HI�������÷�ӦΪ��Ӧǰ�������������ķ�Ӧ������HI�������ﵽƽ��ʱ��ƽ����ԭƽ����ͬ�����Ը����ʵİٷֺ������䣬����Ũ������
A�����ں����ܱ����������г�ʼ����������ѹǿ���A����
B�����ں����ܱ����������г�ʼ���������Ԣ���I2��Ũ����ٺ͢�����ȫ��ͬ�ĵ�Чƽ�⣬����I2��Ũ����ͬ������ƽ��ʱ��I2��Ũ�ȣ��ڣ���=�ۣ���B��ȷ��
C���٢ڢ۶��ǵ�Чƽ�⣬����������I2�����������ͬ����C��ȷ��
D�����ڢ��г�ʼ������ӦŨ�ȴ�Ӧ���ʿ죬���Ե���ƽ������ʱ����̣����Ԣڣ��ۣ���D����
��ѡ��BC��
���� ���⿼���˵�Чƽ�⣬��ѧƽ���Ӱ�����أ��ѶȽϴ�ע����ȫ��ͬ�ĵ�Чƽ����һ��ĵ�Чƽ�������


 ����ν����Ž̲��㽭���̴�ѧ������ϵ�д�
����ν����Ž̲��㽭���̴�ѧ������ϵ�д� �����Ļ������������������ϵ�д�
�����Ļ������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6�� | B�� | 7�� | C�� | 8�� | D�� | 9�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
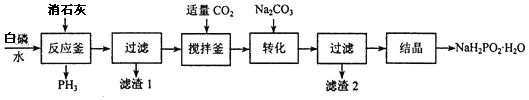
 �����£���0.100mol/L NaOH ��Һ�ֱ�ζ�20.00mL 0.100mol/L������ʹ��ᣬ�ζ�������ͼ��ʾ������˵����ȷ���ǣ�������
�����£���0.100mol/L NaOH ��Һ�ֱ�ζ�20.00mL 0.100mol/L������ʹ��ᣬ�ζ�������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ��ֱ��ʾ����ʹ���ĵζ����� | |
| B�� | pH=7ʱ������������NaOH��Һ�������� | |
| C�� | V��NaOH��=10.00 mL ʱ$\frac{c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COO��}$��1 | |
| D�� | V��NaOH��=20.00 mL ʱ��c��Cl-����c��CH3COO-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� | C-C | C-H | O=O | H-O | C-O | C=O |
| ����/��kJ•mol-1�� | 348 | 413 | 498 | 463 | 351 | 799 |
| ʵ���� | ʵ�鲽�� | ʵ������ |
| 1 | ��4mL��ˮ�Ҵ��м���1mL��ˮ�����������4Сʱ | ��Һ�Ȼ�ɫ��ȥ����Һ�ӽ���ɫ |
| 2 | ��4mL��ˮ�Ҵ��м���1mL��ˮ������������ | ��ʼ�������ԣ����ں���ҺѸ����ɫ |
| �����KI��Һ�еμ���ȴ����������Һ | ��Һ��ɫ���� | |
| 3 | ��4mLˮ�м���1mL��ˮ������������ | �Ȼ�ɫ�Ա�dz |
| �����KI��Һ�еμ���ȴ�����ˮ���Һ | ��Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ֱ�ȡ���ֹ�����Ʒ�����Ȳ����������̼������ | |
| B�� | �ֱ�ȡ������ˮ������Ȼ�����Һ�����а�ɫ��������̼���� | |
| C�� | �ֱ�ȡ������ˮ��������ʯ��ˮ�����а�ɫ��������̼���� | |
| D�� | �ֱ�ȡ�����������ֹ�����Ʒ�������������ᷴӦ����������϶����̼������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ɼ�������KMnO4��Һ���𱽡��Ҵ������Ȼ�̼ | |
| B�� | ̼������Һ����������Һ�����ж����ЧӦ | |
| C�� | ú�ĸ���ʯ�͵ķ�����֬��ˮ�ⶼ�ǻ�ѧ�仯 | |
| D�� | ������ϡ������Һ���Ⱥ����������Һ����ˮԡ���Ȳ���������֤������ˮ��������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com