
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:选择题
| A. | 质子数A>B>C>D | B. | 原子半径D>C>A>B | ||
| C. | 氢化物的稳定性H2D>HC | D. | 碱性的强弱AOH>B(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X、Y元素的金属性X>Y | |
| B. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| C. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| D. | 一定条件下,W单质不能将Z单质从其氢化物中置换出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
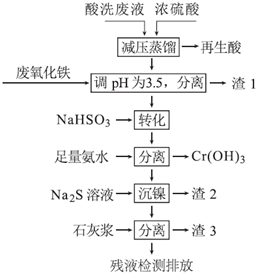
| Fe3+ | Ni2+ | Cr3+ | |
| 开始沉淀 | 1.5 | 6.7 | 4.0 |
| 沉淀完全 | 3.4 | 9.5 | 6.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl元素的相对原子质量为37 | |
| B. | $\frac{1}{20}$mol的1H37Cl分子所含中子数约为6.02×1023 | |
| C. | 7.4 g的37Cl2气体的体积为2.24L | |
| D. | 37Cl2气体的摩尔质量为74g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若3<m<8,则X必定为主族元素 | |
| B. | 若a<b且m=n=4,X、Y不可能形成化合物 | |
| C. | Y的气态氢化物的分子式为H8-nY | |
| D. | 若a=b=3,8>m>n>5,则元素非金属性:X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | C-H | O-O | O=O | C-0 | C=O | H-O |
| 能量(KJ) | 415 | 138 | 498 | 343 | 798 | 465 |
| A. | 放出热量800kJ | B. | 放出热量1520kJ | C. | 吸收热量410kJ | D. | 放出热量610kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | a、b、c的简单离子中,b的离子半径最大 | |
| B. | c、d、f最高价氧化物对应的水化物两两之间均可发生反应 | |
| C. | e的氢化物比f的氢化物的稳定性高 | |
| D. | 离子半径a3-小于d3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,22.4LH2的分子数为1NA | |
| B. | 0 5mol•L-1的MgCl2溶液,含有Cl数为1NA | |
| C. | 56g铁片投人足量的浓硫酸中生成1.5NA个SO2分子 | |
| D. | 常温常压下,14gN2含有分子数为0.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com