
ij������ȤС����е��ԭ����ʵ��̽�����������µ�ʵ�飺��ͭΪ�缫������ͼ��ʾ��װ�õ�ⱥ��ʳ��ˮ��

ʵ������ͨ��Դ30 s�ڣ������������ְ�ɫ���ǣ�֮���ɳȻ�ɫ���ǣ���ʱ�ⶨ��Һ��pHԼΪ10��һ��ʱ����Թܵײ��ۼ�������ɫ��������Һ��Ϊ��ɫ��
�������ϣ�
���� | �Ȼ�ͭ | ������ͭ | ��������ͭ(���ȶ�) | �Ȼ���ͭ |
��ɫ | �������ɫ��Ũ��Һ����ɫ��ϡ��Һ����ɫ | ��ɫ | �Ȼ�ɫ | ��ɫ |
*��ͬ�¶���CuCl���ܽ�ȴ���CuOH
����˵���������
A����Ӧ������������Һ�ʼ���
B�������Ϸ����ĵ缫��ӦΪ��2H2O + 2e? �T H2��+ 2OH?
C������������������������
D���Թܵײ���ɫ�Ĺ�����л�ԭ��
 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д� Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������Զһ�С�����һ�и߶��ϵڶ���������ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪����N��N 946 kJ/mol ,H��H 436kJ/mol ,N��H 391 kJ/mol���������ϼ���2NH3��g�� N2(g)+3H2(g)�ĨSHΪ
N2(g)+3H2(g)�ĨSHΪ
A����46 kJ/mol B����92 kJ/mol
C����92 kJ/mol D����1800kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶���12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�0.1 mol��L��1��HA��Һ��pH��3�������Һ����μ���NaOH��Һ���ڵμӹ����У��й�������ȷ����
A��ԭHA��Һ�У�c(H��)��c(OH��)��c(A��)
B��������������NaOH���ٽ���HA�ĵ��룬��Һ��pH����
C����ǡ����ȫ�к�ʱ����Һ������
D����NaOH��Һ����ʱ�����ܳ��֣�c(A��)>c(Na��)>c(OH��)>c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ������ѧ�ڰ��ڿ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ں���FeCl3��BaCl2��������Һ�У�ͨ��������SO2���а�ɫ�������ɣ����˺�����Һ�еμ�KSCN��Һ������������������������ȷ����
A����ɫ��������BaSO3 B����Һ�����Լ���
C����ɫ������BaSO4 D��FeCl3ȫ������ԭΪFeCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ������ѧ�ڰ��ڿ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ��Na2O2��SO2=Na2SO4��Ƚϣ�Na2O2��������ͬ����
A��2Na2O2��2CO2=2Na2CO3��O2�� B��2Na2O2��2SO3=2Na2SO4��O2
C��Na2O2��H2SO4=Na2SO4��H2O2 D��3Na2O2��Cr2O3=2Na2CrO4��Na2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����ϰ��ڿ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA���������ӵ�����������˵����ȷ����
A��14g C2H4��C4H8�Ļ�������������Ĺ��ۼ���Ϊ 3NA
B����״���£�11.2 L SO3�����ķ�����Ϊ0.5 NA
C��24g 3H218O���е�������Ϊ12NA
D��0.1 mol O22-�����ĵ�����Ϊ1.6NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ�ڵڶ��μ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ˮ���������˵����ȷ����
A��25�棬pH=12���ռ���Һ�봿����Һ��ˮ�ĵ���̶���ͬ
B�������������䣬ϡ�ʹ�������Һ��ˮ�ĵ���̶�����
C�������������䣬ϡ������������Һ��ˮ�ĵ���̶ȼ�С
D�������������䣬�¶����ߣ�ˮ�ĵ���̶�����Kw����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������˳����ȫ��ȷ�������
���ܽ��ԣ�Na2CO3��NaHCO3��MgCO3��Mg(OH)2
�ڵ�Ũ�ȵ���������Һ��pH��ϵ��NaAlO2��NaHCO3��NaClO
�۳����£���a1��a2��a3�ֱ��ʾpH=2�����ᡢpH=12�İ�ˮ��pH=12��̼������Һ��ˮ�ĵ���̶ȣ���a1=a2��a3
��ͬ���£�1L0.5mol/L NH4Cl��Һ��n(NH4��)��2L 0.25mol/LNH4Cl��Һ��n(NH4��)���ֱ�Ϊa��b����a��b
�����ȶ��ԣ�H2O��H2Se��H2S
�ް뾶��Cl����O2����Al3+��F��Si��Na
�������ԣ�MnO2��Cl2��Fe3����Cu2��
��е㣺���ʯ���Ȼ��ƣ��ɱ���������
A���٢ڢۢܢ� B���٢ۢܢޢߢ� C���ڢݢ� D���٢ܢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶�12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ�д��ڵ���ƽ�⣺CH3COOH  CH3COO- + H+ ������������ȷ����
CH3COO- + H+ ������������ȷ����
A��CH3COOH��Һ������Ũ�ȵĹ�ϵ���㣺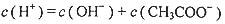
B��0��1 mol / L ��CH3COOH ��Һ��ˮϡ�ͣ���Һ��c(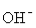 )��С
)��С
C��CH3COOH��Һ�м�������CH3COONa���壮ƽ�������ƶ�
D�������£�pH��2��CH3COOH��Һ��pH��12��NaOH ��Һ�������Ϻ���Һ��pH��7
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com