
����Ŀ��(1)���������õ������£�NH4+����������Ӧ��������NO3-��������Ӧ�������仯ʾ��ͼ���£�

1 mol NH4+(aq)ȫ��������NO3-(aq)���Ȼ�ѧ����ʽ��___________________��
(2)��ҵ�ϳ���CO��H2�ϳɼ״�����Ӧ����ʽΪ��CO(g) ��2H2(g)![]() CH3OH (g)����H����T1ʱ�����Ϊ2 L�ĺ��������г������ʵ���֮��Ϊ3 mol��H2��CO���ﵽƽ��ʱCH3OH���������(V %)��n(H2)/n(CO)�Ĺ�ϵ��ͼ1��ʾ��
CH3OH (g)����H����T1ʱ�����Ϊ2 L�ĺ��������г������ʵ���֮��Ϊ3 mol��H2��CO���ﵽƽ��ʱCH3OH���������(V %)��n(H2)/n(CO)�Ĺ�ϵ��ͼ1��ʾ��

�ٵ���ʼn(H2)/n(CO)��2������5 min�ﵽƽ�⣬��ʱ������ѹǿ�dz�ʼѹǿ��0.7������0��5 min��ƽ����Ӧ����v(H2)��________������ʱ���������м���0.15 mol CO (g)��0.05 mol CH3OH(g)������ƽ��ʱH2��ת���ʽ�________(��������������С������������)��
�ڵ���ʼn(H2)/n(CO)��3.5ʱ���ﵽƽ��״̬��CH3OH���������������ͼ���е�____��(����D����E������F��)��
����ͼ2��֪�÷�Ӧ����H________0(����>����<����������)��������______________����ѹǿΪp2ʱ����y�㣺v��________v��(����>����<����������)��
���𰸡�NH4+��aq��+2O2��g���T2H+��aq��+H2O��l��+NO3-��aq������H=-346 kJ/mol 0.09mol/(L.min) ���� F > �¶����ߣ�һ����̼��ת��������ƽ��������� >
��������
��1�����ͼ����ݸ�˹���������㷴Ӧ���ʱ䣻
��2������CO�����������ʵ���n(H2)/n(CO)��2
���Լ���CO���������Ե����ʵ�������������ʽ����ƽ��ʱ��������ʵ�������������ʵ����仯��������v=c��t������v��H2����
�ȼ�����¶���ƽ�ⳣ��K���ټ���Ũ����Qc����ƽ�ⳣ��K����жϷ�Ӧ���з���������ȷ������ת���ʱ仯��
�ڻ�ϱ������ڻ�ѧ������֮��ʱ��ƽ��ʱ������ĺ������
��1����һ�����Ȼ�ѧ����ʽΪNH4+��aq��+1.5O2��g���TNO2-��aq��+2H+��aq��+H2O��l������H=-273KJ/mol��
�ڶ������Ȼ�ѧ����ʽΪ��NO2-��aq��+0.5O2��g���TNO3-��aq������H=-73KJ/mol��
���ݸ�˹������NH4+��aq��+2O2��g���T2H+��aq��+H2O��l��+NO3-��aq������H=-346 kJ/mol��
�ʴ�Ϊ��NH4+��aq��+2O2��g���T2H+��aq��+H2O��l��+NO3-��aq������H=-346 kJ/mol��
(2)��H2��CO�ܹ�Ϊ3mol,����ʼn(H2)/n(CO)=2,��֪H2Ϊ2mol��COΪ1mol��5min�ﵽƽ��ʱ��ʱ������ѹǿ�dz�ʼѹǿ��0.7�����������ĵ�һ����̼Ϊxmol��
CO(g) ��2H2(g)![]() CH3OH (g)
CH3OH (g)
��ʼ(mol): 1 2 0
�仯(mol): x 2x x
ƽ��(mol): 1-x 2-2x x
(1-x+2-2x+ x)��3=0.7 ��ã�x=0.45
�������ݻ�Ϊ2L,��v(H2)=0.9mol��2L��5min=0.09mol/(L.min)��
���¶���ƽ�ⳣ��K=0.225��(0.275��(0.55)2),��ʱ����������0.15 mol CO (g)��0.05 mol CH3OH(g)����ʱŨ����Qc=0.25��(0.35��(0.55)2)<K=0.225��(0.275��(0.55)2)����Ӧ������Ӧ���У�����ƽ��ʱH2��ת���ʽ�����
�ʴ�Ϊ��0.09mol/(L.min)������
�ڻ�ϱ������ڻ�ѧ������֮��ʱ,ƽ��ʱ������ĺ������,�ʵ�n(H2)/n(CO)��3.5ʱ,�ﵽƽ��״̬��,CH3OH���������С��C�㣬��ѡF��
�ʴ�Ϊ��F��
����ͼ2��֪���ڵ�ѹ���������¶ȵ����ߣ�һ����̼��ת���������������¶ȵ����߷�Ӧ������У�������Ӧ�����ȷ�Ӧ����H>0����ѹǿΪp2ʱ����y��δ����ƽ��״̬����ѹǿ���¶���Ҫ����ƽ��״̬��һ����̼��ת����Ҫ����������Ӧ������У���v��>v��
�ʴ�Ϊ��>���¶����ߣ�һ����̼��ת��������ƽ��������У�>��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����廯�ѣ�TiBr4����������ҵ��ϩ���ۺϷ�Ӧ�Ĵ�������֪TiBr4������Ϊ�Ȼ�ɫ���壬�۵�Ϊ38.3�棬�е�Ϊ233.5�棬���г�����������ˮ�⡣ʵ�������÷�ӦTiO2+C+2Br2![]() TiBr4+CO2�Ʊ�TiBr4��װ����ͼ��ʾ���ش��������⣺
TiBr4+CO2�Ʊ�TiBr4��װ����ͼ��ʾ���ش��������⣺
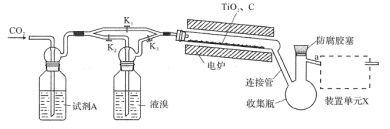
��1�����װ�������Բ�����ҩƷ����ǰӦ���еIJ�����__����Ŀ����__����ʱ����K1��K2��K3��״̬Ϊ__��һ��ʱ���¯�����ȷ�Ӧ�ܣ���ʱ����K1��K2��K3��״̬Ϊ____��
��2���Լ�AΪ__��װ�õ�ԪX��������__����Ӧ������������Դ��Ъ�������ӹܣ���Ŀ����___��
��3����Ӧ������Ӧ����ͨ��һ��ʱ��CO2����ҪĿ����___��
��4�������ӹ��жϲ��۷⣬���������ᴿ����ʱӦ��a�˵�������װΪ__���нӹܺͽ���ƿ���ڷ��������ϼ�װ��������___�����������ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��C(s)+O2(g) ![]() CO2(g) ��H=��437.3 kJ��mol-1��2CO(g)+ O2(g)
CO2(g) ��H=��437.3 kJ��mol-1��2CO(g)+ O2(g) ![]() 2CO2(g) ��H=��566.0 kJ��mol-1
2CO2(g) ��H=��566.0 kJ��mol-1
��1��һ����̼�ı�ȼ������HΪ��_________
��2��̼��������Ӧ����һ����̼���Ȼ�ѧ����ʽ�ǣ�___________
��3����ӦCO2(g) + C(s)![]() 2CO(g) ��HΪ��_________________
2CO(g) ��H��_________________
��4����ȫȼ����ͬ���ʵ�����C��CO���ų�������_____�ࣨ��C��CO��
��5����25����101kPaʱ��8gCH4��ȫȼ������Һ̬ˮʱ�ų���������445.15kJ����CH4ȼ�յ��Ȼ�ѧ����ʽ________
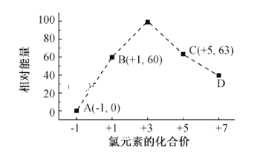
��6��һ�������£���ˮ��Һ��1 mol Cl-��ClOx- (x=1��2��3��4)������(kJ)��Դ�С��ͼ ��ʾ��B��A+C��Ӧ���Ȼ�ѧ����ʽΪ(�����ӷ��ű�ʾ)___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�������Һ����Ũ�ȹ�ϵһ����ȷ���ǣ� ��
A.0.1mol��L��1Na2CO3��Һ�У���ˮϡ�ͣ�![]() ��ֵ��С
��ֵ��С
B.0.1mol��L��1����������Һ�У�c(SO42-)>c(Al3��)>c(H��)>c(OH��)
C.pH��7�İ�ˮ���Ȼ�淋Ļ����Һ�У�c(Cl��)>c(NH4+)
D.pH��2�Ĵ�����Һ��pH��12��NaOH��Һ�������ϣ�c(Na��)��c(CH3COO��)��c(CH3COOH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����ɫ���������Ӧ����������Ϣ�����壮����ӽṹ��![]() ���ƣ���
���ƣ���![]() �����ܱ�
�����ܱ�![]() �����ܵ͡������жϴ������
�����ܵ͡������жϴ������
A.![]() ���ӳ�����������
���ӳ�����������
B.![]() �����ǷǼ��Է���
�����ǷǼ��Է���
C.��Ϊ![]() �����ܱ�
�����ܱ�![]() �����ܵͣ�����
�����ܵͣ�����![]() �е����
�е����![]() �е�
�е�
D.![]() �����ȶ��Ե���
�����ȶ��Ե���![]() ���ӣ���Ϊ
���ӣ���Ϊ![]() �����ܸ�
�����ܸ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ���ѧ����������(�������������黯����)���³����������о���ȡ������Ҫ�ɹ������о���Ŀ�ٻ�2013�����������Ȼ��ѧ����һ�Ƚ���
��1����̬Fe2+�ĺ�������Ų�ʽΪ_________________��
��2����������������Ԫ���е縺��ֵ�ɴ�С��˳����__________(����Ӧ��Ԫ�ط������)��
��3��Fe(SCN)3��Һ�м���NH4F���������·�Ӧ��Fe(SCN)3+6NH4F=(NH4)3FeF6+3NH4SCN��
��(NH4)3FeF6���ڵ����������������ۼ����_________(ѡ����ţ���ͬ)��
a����λ�� b����� c�������� d�����Ӽ�
����֪SCNһ�и�ԭ������������8�����ȶ��ṹ����Cԭ�ӵ��ӻ���ʽΪ_____________,��ԭ������![]() ����
����![]() �����ı�ֵΪ___________________��
�����ı�ֵΪ___________________��
��4��FeCl3����������ˮ���Ҵ����þƾ��Ƽ��ȼ�����������FeF3�����۵����1000�����Խ������ֻ������۵����ϴ��ԭ��_______________________________��
��5�������ס�����Ϊͬ����Ԫ�أ����仯����Ľṹ�������Ƕ������ġ�
�������⻯��RH3(NH3��PH3��AsH3)��ij��������R�ĺ˵�����ı仯��������ͼ��ʾ����Y��ɱ�ʾ���⻯��(RH3)���ʿ�����________��
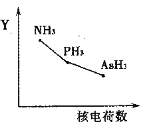
a���ȶ��� b���е� c��R��H���� d�����Ӽ�������
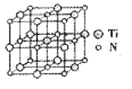
��̼�����ѻ���������������ͺ��պ���������й㷺��Ӧ�ã���ṹ����̼ԭ��ȡ�������Ѿ���(�ṹ��ͼ)����ĵ�ԭ�ӣ��ݴ˷���������̼�����ѻ�̨��Ļ�ѧʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N2O5��һ����������������һ���¶��¿ɷ������з�Ӧ��2N2O5(g) ![]() 4NO2(g) + O2(g) ��H ��+Q kJ/mol (Q>0)��ij�¶��£���2L���ܱ�������ͨ��N2O5������ʵ�����ݼ��±���
4NO2(g) + O2(g) ��H ��+Q kJ/mol (Q>0)��ij�¶��£���2L���ܱ�������ͨ��N2O5������ʵ�����ݼ��±���
ʱ��/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/mol/L | 5.0 | 3.5 | 2.5 | 2.5 |
����˵����ȷ����
A. 500s��N2O5�ֽ�����Ϊ6��10-3mol/(L��s)
B. ���¶��µ�ƽ�ⳣ��K ��125
C. ��Ӧ��ƽ��ʱ�����յ�����Ϊ5Q kJ
D. �����������䣬����ʼʱc(N2O5)��10mol/L�����ƽ���c(N2O5)��5mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.HF��HCl��![]() ��
��![]() ���ȶ���������ǿ
���ȶ���������ǿ
B.��Mg��Si��N��F��˳��ԭ�Ӱ뾶��С���
C.ij����Ԫ�صĵ�����![]() �������±���ʾ
�������±���ʾ![]() ��λ��
��λ��![]() �����Ʋ��Ԫ��λ��Ԫ�����ڱ��ڢ�A��
�����Ʋ��Ԫ��λ��Ԫ�����ڱ��ڢ�A��
I | I | I | I | I | I | I |
578 |
|
|
|
|
|
|
D.�ڢ�P��S����![]() ��Ca����
��Ca����![]() ��Si����Ԫ���У�ÿ���е�һ�����ܽϴ��Ԫ�ص�ԭ������֮��Ϊ41
��Si����Ԫ���У�ÿ���е�һ�����ܽϴ��Ԫ�ص�ԭ������֮��Ϊ41
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ��ͼ�ұ�ʾ����Ԫ�ص�ij��������ԭ�������ı仯������˵����ȷ����
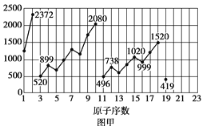

A. ͼ�Ҳ����ܱ�ʾԪ�صĵ縺����ԭ�������ı仯��ϵ
B. ͼ���ܱ�ʾ����Ԫ�ص��ʵ��۵���ԭ�������ı仯��ϵ
C. ͼ�ҿ��ܱ�ʾ����Ԫ��ԭ�ӵİ뾶��ԭ�������ı仯��ϵ
D. ͼ���ܱ�ʾ����Ԫ��ԭ�ӵĵ�һ��������ԭ�������ı仯��ϵ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com