
| A. | K+、Na+、Cl-、NO3- | B. | K+、Na+、Br-、SiO32- | ||
| C. | H+、Fe2+、SO42-、Cl2 | D. | K+、Ag+、NH3•H2O、NO3- |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应,不能结合生成络离子等,则离子大量共存,并结合入CO2后仍能大量共存来解答.
解答 解:A.该组离子之间不反应,可大量共存,且通入CO2后仍不发生反应,能大量共存,故A选;
B.该组离子之间不反应,可大量共存,但通入CO2后与SiO32-反应生成硅酸沉淀,不能共存,故B不选;
C.H+、Fe2+、Cl2发生氧化还原反应,不能共存,故C不选;
D.Ag+、NH3•H2O结合生成沉淀或络离子,不能大量共存,故D不选;
故选A.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
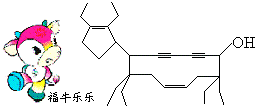
| A. | 牛式二烯炔醇含有4种官能团 | |
| B. | 牛式二烯炔醇不能使酸性KMnO4溶液褪色 | |
| C. | 1 mol牛式二烯炔醇最多可跟4mol Br2发生加成反应 | |
| D. | 该有机物的化学式为C29H44O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解质溶液的导电性强弱是由浓度决定的 | |
| B. | 弱电解质和强电解质的导电,都是由带电离子的定向移动引起的 | |
| C. | 强电解质溶液导电能力强,弱电解质溶液导电能力弱 | |
| D. | 导电性强的溶液中的自由移动离子数目一定比导电性弱的溶液中的自由移动离子数目多 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 向100mL 3mol•L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.
向100mL 3mol•L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 17gNH3中含有的质子数为10NA | |
| B. | 标准状况下,22.4LCl2与56gFe反应生成FeCl2分子的数目为NA | |
| C. | 7.0g丁烯含有C-H键的数目为NA | |
| D. | 常温下,1.0LpH=1的H2SO4溶液中,由水电离出的0H-的数目为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com