
| A. | 2Na2O2+2Mn2O7→4NaMnO4+O2↑ | B. | 2Na2O2+P2O3→Na4P2O7 | ||
| C. | 2Na2O2+2 N2O3→NaNO2+O2↑ | D. | 2 Na2O2+2 N2O5→4NaNO3+O2↑ |
分析 题给信息为:Na2O2可与某些元素的最高价氧化物反应,生成对应的盐(或碱)和O2,Na2O2具有强氧化性,与所含元素不是最高价态的氧化物反应时,只生成相对应的盐,不生成O2.
解答 解:A、七氧化二锰是最高价态的锰的氧化物,NaMnO4中的锰为+7价,符合上述规律,故A正确;
B、三氧化二磷不是最高正价,生成Na4P2O7,符合上述规律,故B正确;
C、三氧化二氮不是最高价态的氮的氧化物,不符合上述规律,故C错误;
D、五氧化二氮是最高价态的氮的氧化物,因此过氧化钠与五氧化二氮反应生成硝酸钠和氧气,故D正确;
故选C.
点评 本题根据题目信息得出规律,主要考查化学方程式的书写,理解反应规律是解题关键,难度较大.


科目:高中化学 来源: 题型:多选题
| A. | 加催化剂,v(正)和v(逆)都发生变化,且变化的倍数相等 | |
| B. | 加压,v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数 | |
| C. | 降温,v(正)和v(逆)都减少,且v(正)减少倍数大于v(逆)减少倍数 | |
| D. | 增加c(N2),v(正)和v(逆)都增大,且v(正)增加倍数大于v(逆)增加倍数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 固体质量 | 加入某浓度盐酸的体积/mL | 加入某浓度NaOH的体积/mL | 收集到气体体积/mL |
| 1 | 0.9 | 20.0 | ─ | 1008 |
| 2 | 0.9 | 30.0 | ─ | 1008 |
| 3 | 0.9 | ─ | 20.0 | 672 |
| 4 | 0.9 | ─ | 30.0 | 672 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(mg) | 255 | 385 | 459 |
| 标准状况下气体的体积(mL) | 280 | 336 | 336 |
| A. | 甲、乙组的实验中,盐酸均是过量的 | B. | 盐酸的物质的量浓度为0.8mol L-1 | ||
| C. | 合金中镁、铝的物质的量之比为1:1 | D. | 丙组中铝的物质的量为0.0045mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 气体 | CO2 | HCl | HCl | SO2 |
| 液体 | H2O | NaOH | H2O | NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
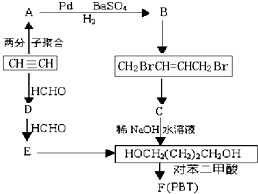 请根据以下知识解答
请根据以下知识解答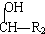 (R代表烃基,下同.)
(R代表烃基,下同.)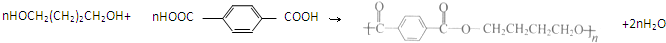 .
.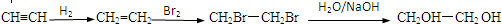 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
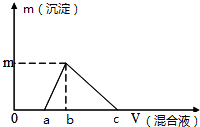 往100mL0.1mol/L NaOH溶液中逐滴滴入浓度均为0.1mol/L的氯化铝和盐酸的混合溶液,测得生成沉淀的质量(g)与滴入的混合液的体积(mL)的关系如图所示,则下列说法正确的是( )
往100mL0.1mol/L NaOH溶液中逐滴滴入浓度均为0.1mol/L的氯化铝和盐酸的混合溶液,测得生成沉淀的质量(g)与滴入的混合液的体积(mL)的关系如图所示,则下列说法正确的是( )| A. | a=25mL | B. | b=33mL | C. | c=100mL | D. | m=0.195g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3固体 | B. | 3 mol•L-1的H2SO4溶液 | ||
| C. | CH3COOK溶液 | D. | KNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com