
分析 (1)使水的电离平衡向右移动的方法有:升高温度、加入含有弱根离子的盐等,如果溶液呈酸性,说明加入的物质和氢氧根离子反应,导致溶液中氢氧根离子浓度小于氢离子浓度而使溶液呈酸性;
(2)100℃沸水显示中性,根据中性环境下pH试纸的颜色来确定即可;在25℃时,水的pH=7,温度升高,则pH增大,水在任何温度下均为中性;
(3)①向氨水中加入硫酸铵,抑制一水合氨电离;
②溶液呈中性,则c(H+)=c(OH-),根据电荷守恒判断离子浓度;
③若向氨水中加入硫酸,二者恰好反应生成硫酸铵,硫酸铵是强酸弱碱盐,其溶液呈酸性;
④0.1mol•L-1的氨水与pH=1的硫酸混合,硫酸浓度为0.5mol/L,且氨水与硫酸的体积比为1:1,生成硫酸铵.
解答 解:(1)A.向水中加入Al2(SO4)3,强酸弱碱盐能水解,铝离子和氢氧根离子结合生成氢氧化铝,从而促进水电离,导致溶液中C(OH-)<C(H+),溶液呈酸性,故A正确;
B.在水中加入NaHSO4,溶解后电离出氢离子,抑制水电离,平衡向左移动,且溶液中C(H+)>C(OH-),溶液呈酸性,故B错误;
C.水的电离是吸热反应,加热至100℃,促进水电离,溶液C(OH-)=C(H+),溶液呈中性,故C错误;
D.在水中加入Na2CO3,促进水的电离,C(H+)<C(OH-),水解显碱性,故D错误;
故答案为:A;
(2)100℃沸水仍然是中性的,pH试纸测定溶液的酸碱性时,中性溶液不变色,所以是淡黄色的,温度升高会促进水的电离,所以水的pH会减小,pH=6<7为中性,水在任何温度下均为中性的,若用pH计测定,则溶液呈中性;
故答案为:淡黄;中;<;中;
(3)①向氨水中加入硫酸铵,铵根离子浓度增大抑制一水合氨电离,平衡向左移动,则氢氧根离子物质的量减小,一水合氨分子物质的量增大,所以溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ 减小,故答案为:减小;
②混合溶液呈中性,所以c(H+)=c(OH-),根据电荷守恒得c(NH4+)+c(H+)=2c(SO42-)+c(OH-),所以c(SO42-)=$\frac{1}{2}$c(NH4+)=$\frac{1}{2}$amol•L-1,
故答案为:$\frac{1}{2}$amol•L-1;
③若向氨水中加入硫酸,二者恰好反应生成硫酸铵,反应的离子方程式为NH3•H2O+H+=NH4++H2O,硫酸铵为强酸弱碱盐,铵根离子水解而使其溶液呈酸性,pH<7,水解离子方程式为NH4++H2O?NH3•H2O+H+,溶液呈酸性则c(H+)>c(OH-),
故答案为:NH3•H2O+H+=NH4++H2O;<;NH4++H2O?NH3•H2O+H+;
④0.1mol•L-1的氨水与pH=1的硫酸混合,硫酸浓度为0.5mol/L,且氨水与硫酸的体积比为1:1,生成硫酸铵,溶液中存在电荷守恒c(H+)+c(NH4+)=2c(SO42-)+c(OH-),c(NH4+)>c(SO42-),铵根离子水解程度较小,所以c(SO42-)>c(H+),则离子浓度大小顺序是 c(NH4+)>c(SO42-)>c(H+)>c(OH-),
故答案为:c(NH4+)>c(SO42-)>c(H+)>c(OH-).
点评 本题考查弱电解质的电离平衡,为高频考点,把握电离平衡移动、酸碱混合计算为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:解答题
 肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题: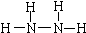 .
.| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(N2) | n(H2) | n(NH3) | |
| 甲 | 1mol | 3mol | 0mol |
| 乙 | 0.5mol | 1.5mol | 1mol |
| 丙 | 0mol | 0mol | 4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
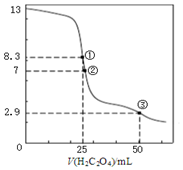 25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )
25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )| A. | 点①所示溶液中:c(H+)+2c(H2C2O4)+c(HC2O4-)=c(OH-) | |
| B. | 点②所示溶液中:c(HC2O4-)+2c(C2O42-)=0.0500mol•L-1 | |
| C. | 点③所示溶液中:c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| D. | 滴定过程中可能出现:c(Na+)>c(C2O42-)=c(HC2O4-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 表中是不同温度下水的离子积的数据:
表中是不同温度下水的离子积的数据:| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
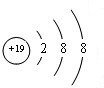
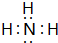 ;⑨的最高价氧化物对应的水化物
;⑨的最高价氧化物对应的水化物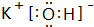 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
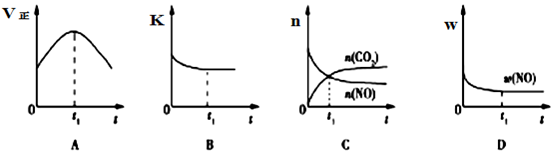
| 物质 温度/℃ | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
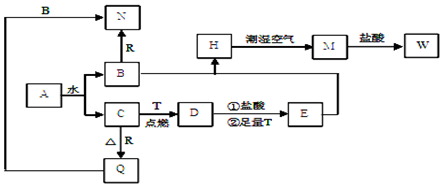

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径Y>Z>X | |
| B. | X分别与Y、Z形成的化合物均至少有两种 | |
| C. | 最高价氧化物对应水化物的酸性:W>Z | |
| D. | 氢元素在与X、Y、Z分别形成的化合物中,化合价均为+1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com