
【题目】某溶液中含有HCO3﹣、SO32﹣、Cl﹣和Na+ , 若向其中通入足量的Cl2 , 溶液中上述四种离子的浓度基本保持不变的是( )
A.HCO3﹣
B.SO32﹣
C.Cl﹣
D.Na+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列物质的保存方法正确的是
A.氢氧化钠溶液保存在玻璃塞的玻璃瓶中
B.漂白粉露置于空气中
C.浓硝酸、氯水保存在棕色细口玻璃瓶中
D.钠保存在盛有水的试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C和Si元素在化学中占有极其重要的地位:
(1)写出Si的基态原子核外电子排布式 . 从电负性角度分析,C,Si和O元素的非金属活泼性由强至弱的顺序为 .
(2)CO2分子的空间构型为 , 中心原子的杂化方式为 , 和CO2 互为等电子体的氧化物是 .
(3)C,Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同.CO2中C与O原子间原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键.从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键.
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为 , 在SiC中,每个C原子周围最近的C原子数目为 , 若晶胞的边长为a pm,则金刚砂的密度为 . 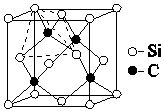
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300mL Al2(SO4)3溶液中,含Al3+为1.62g,在该溶液中加入0.1mol·L-1Ba(OH)2溶液300mL,反应后溶液中SO42﹣的物质的量浓度为( )
A. 0.4mol·L-1 B. 0.3mol·L-1 C. 0.2mol·L-1 D. 0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的四种短周期元素,A2﹣和B+具有相同的电子构型,C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子. 回答下列问题:
(1)C原子的核外电子排布式为 .
(2)单质A有两种同素异形体,其中沸点高的是(填分子式),原因是;A、B、D三元素组成的化合物所属的晶体类型是 .
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为 , 中心原子的杂化轨道类型为 .
(4)A和B能够形成化合物1:1的化合物,写出此化合物的电子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取5.48gNa2CO3和NaHCO3的混合物溶于水配成200mL溶液,将溶液分成两等份。
(1)往其中一份溶液中加入300mLBa(OH)2溶液时,恰好使生成白色沉淀的量最多,测得反应后溶液的c(OH-)=0.100mol·L-1 (混合溶液体积改变忽略不计),则原混合物中n(Na2CO3) : n(NaHCO3)=。
(2)往另一份溶液中缓慢滴加0.l00mol·L-1盐酸,当加入的盐酸体积为300mL时,则收集到的CO2气体在标准状况下的体积为L(不考虑CO2在水中的溶解)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项除杂所用方法正确的是 ( )
A. KCl固体混有KClO3:加少量二氧化锰固体并加热
B. CO2中混有CO气体:通入氧气中点燃
C. 硝酸钾溶液中混有氯化钠:加入四氯化碳萃取并分液
D. Cu(NO3)2溶液混有AgNO3:加入过量的铜粉并过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是自然賜给人类的宝藏,海水的综合利用是全世界研究的重点。
完成下列问题:
(1)粗盐中除了含有泥沙之外还含有Ca2+、Mg2+、SO42-等杂质,粗盐获得精盐一般步骤:

加入氯化钡、纯碱和烧碱的目的依次是:_________、_________、_________。
(2)海水提取金属镁流程如下:

流程中加入熟石灰目的__________;沉淀与盐酸反应的离子方程式_____________。
(3)某学生实验室模拟河水提取溴的步骤为:海水→浓缩→氧化→提取→溴
①氧化步骤:适宣作氧化剂的是_______。
ABr2 B.Cl2 C.I2 DHCl
②提取步骤:……溴水中加入CCl4振荡、静置……得溴的四氯化碳溶液,该分离提纯溴的方法叫________;用到的主要仪器为________。
(4)实验证明金属制品在海水中更容易生锈,铜锈的化学式为: ________;Cu与硫磺反应的化学方程式________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com