
| A. | 分别加热两种样品,没有残留物质是NaHCO3 | |
| B. | 分别配成溶液,再加入石灰水,无白色沉淀生成的是NaHCO3 | |
| C. | 分别配成溶液,向其中逐滴加入同浓度的盐酸反应,先产生CO2的是NaHCO3 | |
| D. | 二者在一定条件下不能相互转化 |
分析 A、依据碳酸氢钠加热分解生成碳酸钠固体、二氧化碳和水分析;
B、碳酸钠、碳酸氢钠都能够与澄清石灰水反应生成白色沉淀碳酸钙;
C、根据碳酸氢钠直接反应生成二氧化碳,而碳酸钠先生成碳酸氢钠后再生成二氧化碳分析;
D、碳酸氢钠加热分解生成碳酸钠,碳酸钠溶液中通入二氧化碳能够生成碳酸氢钠.
解答 解:A、碳酸氢钠加热分解生成了固体碳酸钠,有残留的物质存在,故A错误;
B、由反应Na2CO3+Ca(OH)2═CaCO3↓+2NaOH、2NaHCO3+Ca(OH)2═Na2CO3+CaCO3↓+2H2O可知,澄清的石灰水与碳酸钠、碳酸氢钠都反应生成白色沉淀碳酸钙,故B错误;
C、碳酸钠与盐酸反应,先生成碳酸氢钠,然后碳酸氢钠再与盐酸反应生成二氧化碳,而碳酸氢钠直接与盐酸反应生成二氧化碳,所以反应生成二氧化碳的速率碳酸氢钠的大于碳酸钠的,故C正确;
D、碳酸钠溶液中通入二氧化碳,碳酸钠能够转化成碳酸氢钠,碳酸氢钠加入分解能够生成碳酸钠,所以二者能够相互转化,故D错误,
故选C.
点评 该题考查碳酸钠与碳酸氢钠的性质比较,是高考中的常见题型,该题基础性强,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和应试能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 18gD2O和18gH2O中含有的质子数均为10NA | |
| B. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA | |
| C. | 2L0.5mol/L亚硫酸溶液中含有的氢离子数为2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由题目信息知:KMnO4的氧化性比MnO2的强 | |
| B. | 制备氯气的整个实验过程中,只需要使用氧化剂与还原剂 | |
| C. | 用排气法收集不需要利用其他试剂就能确定集气瓶中已收集满气体 | |
| D. | 用足量MnO2与含有4 molHCl的浓盐酸在加热条件下反应,得到Cl2的物质的量小于1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①② | C. | ③④ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在101 k Pa时,1 mol C与适量O2反应生成1mol CO时,放出110.5 kJ热 量,则C的燃烧热为110.5 kJ/mol | |
| B. | 在10l k Pa时l mol H2完全燃烧生成液态水放出285.8 kJ热量,H2燃烧热为-285.8kJ/mol | |
| C. | 鉴定HCl和NaOH反应的中和热时,每次实验均应测量3个温度即盐酸起始温度、NaOH起始温度和反应后终止温度 | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3KJ/mol,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
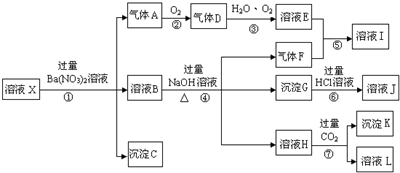
 ,沉淀K的化学式为:Al(OH)3,沉淀G的化学式为:Fe(OH)3,实验中,可以观察到反应②的现象是:气体由无色变红棕色.
,沉淀K的化学式为:Al(OH)3,沉淀G的化学式为:Fe(OH)3,实验中,可以观察到反应②的现象是:气体由无色变红棕色.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com