
| A. | 沸点:H2S>H2Se | B. | 熔点:NaCl>CCl4 | ||
| C. | 酸性:HClO4>H2SO4 | D. | 碱性:NaOH>Mg(OH)2 |
分析 A.氢化物的熔沸点与相对分子质量成正比,但含有氢键的氢化物熔沸点较高;
B.离子晶体熔沸点高于分子晶体;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
D.元素的金属性越强,其最高价氧化物的水化物碱性越强.
解答 解:A.氢化物的熔沸点与相对分子质量成正比,但含有氢键的氢化物熔沸点较高,这两种氢化物都不含氢键,且前者相对分子质量小于后者,则熔沸点H2S<H2Se,故A错误;
B.离子晶体熔沸点高于分子晶体,氯化钠是离子晶体,四氯化碳是分子晶体,则熔点:NaCl>CCl4,故B正确;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性Cl>S,则酸性:HClO4>H2SO4,故C正确;
D.元素的金属性越强,其最高价氧化物的水化物碱性越强,金属性Na>Mg,则碱性:NaOH>Mg(OH)2,故D正确;
故选A.
点评 本题考查元素周期律,为高频考点,涉及物质熔沸点判断及元素周期律运用,明确同一周期、同一主族元素原子结构及其性质递变规律是解本题关键,注意氢化物的熔沸点与分子间作用力和氢键有关,与化学键无关.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠溶液中滴入氢氧化钠溶液:CO32-+H++OH-=CO32-+H2O | |
| B. | 浓烧碱溶液中加入铝片:Al+2OH-=AlO2-+H2O | |
| C. | 用NaOH溶液溶解Al2O3:2OH-+Al2O3=2AlO2-+H2O | |
| D. | 向氢氧化钠溶液中通入过量的二氧化碳:CO2+2OH-=CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子由原子核和核外电子构成 | |
| B. | 对于任何微粒,质子数等于核外电子数都成立 | |
| C. | 当微粒达到稳定结构时,最外层电子数一定是8 | |
| D. | 原子的质量等于原子核的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含NA个阴离子的Na2O2溶于水形成1L溶液,其物质的量的浓度为1mol/L | |
| B. | 25g质量分数为68%的H2O2水溶液中含有氧原子数目为NA | |
| C. | 常温常压下,0.1molD2O含有中子数为NA | |
| D. | 用5mL3mol/LFeCl3溶液制成的氢氧化铁胶体中所含胶粒数为0.015 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量10.56gNa2CO3固体--用托盘天平 | |
| B. | 准确量取10.00mL的溶液--用50mL量筒 | |
| C. | 灼烧干海带至完全变成灰烬--用蒸发皿 | |
| D. | 过滤煮沸后的硬水--用普通漏斗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
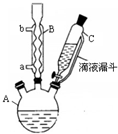 对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图:
对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图: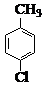 $→_{催化剂}^{KMnO_{4}}$
$→_{催化剂}^{KMnO_{4}}$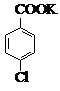 +MnO2
+MnO2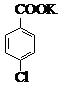
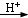
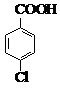
| 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 颜色 | 水溶性 | |
| 对氯甲苯 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 具有盐的通性,属于可溶性盐 | ||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com