
 .有机物X的键线式为:
.有机物X的键线式为:
| 一溴代二甲苯 | 234℃ | 206℃ | 213.8℃ | 204℃ | 214.5℃ | 205℃ |
| 对应二甲苯 | 13℃ | -54℃ | -27℃ | -54℃ | -27℃ | -54℃ |
 的分子式为C8H8;
的分子式为C8H8; 中含有双键能发生聚合反应;
中含有双键能发生聚合反应; 的分子式为C8H8,Y中含有苯环,Y的结构简式:
的分子式为C8H8,Y中含有苯环,Y的结构简式: ,
, ;
; 中含有双键能发生聚合反应:
中含有双键能发生聚合反应: ,
, ;
;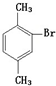 ;
; ;邻二甲苯.
;邻二甲苯.


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
| A、只有硫元素被氧化 |
| B、NO是还原产物 |
| C、还原剂与氧化剂的物质的量之比是3:16 |
| D、0.3mol Cu(NO3)2生成时转移电子0.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,请完成下列问题:
,请完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.5mol |
| B、1.8mol |
| C、1.5mol |
| D、1.2mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com