
| A. | 150 mL 1.5 mo1•L-1NaCl溶液 | B. | 75 mL 3 mol•L-1MgCl2溶液 | ||
| C. | 150 mL 2 mo1•L-1KCl溶液 | D. | 75 mL 1 mol•L-1A1C13溶液 |
分析 氯离子的浓度=溶液的浓度×化学式中氯离子个数,与溶液体积无关.
解答 解:100mL l.5mol•L-1CaCl2溶液中的Cl-浓度为1.5mol/L×2=3mol/L,
A.150mL 1.5mo1.L-1NaCl溶液中氯离子的浓度为1.5mol/L,与题意不符,故A错误;
B.75mL 3mol•L-1MgCl2溶液中氯离子的浓度为3mol/L×2=6mol/L,与题意不符,故B错误;
C.150mL 2mo1.L-1KCl溶液中氯离子的浓度为2mol/L,与题意不符,故C错误;
D.75mL 1mol•L-1A1C13溶液中氯离子的浓度为1mol/L×3=3mol/L,符合题意,故D正确.
故选D.
点评 本题考查了溶液中离子浓度的计算,明确溶液中离子的浓度=溶液的浓度×化学式中离子个数是解本题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 质子数为235 | B. | 中子数为92 | C. | 电子数为143 | D. | 质量数为235 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验要求 | 实验方法 |
| 测定某工业废水的酸碱度 | |
| 检验自来水中残余氯分子 | |
| 检验CO2气体中含有的SO2 | |
| 除去FeCl2中的少量FeCl3 | |
| 除去NO中混有的少量NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,4,8 | B. | 3,4,8 | C. | 2,3,9 | D. | 3,4,9 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | O2和O3互为同素异形体 | B. | O3是由3个氧原子构成的化合物 | ||
| C. | O2和O3相互转化属于化学变化 | D. | O3的摩尔质量为48g.mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
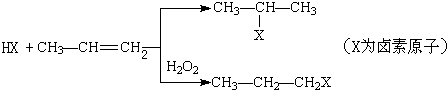

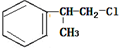 、
、 ;
;
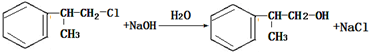
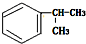 的一种同分异构体D符合以下条件:①苯环上有两条侧链 ②苯环上的一氯代物有2种,则D的结构简式为
的一种同分异构体D符合以下条件:①苯环上有两条侧链 ②苯环上的一氯代物有2种,则D的结构简式为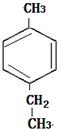 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 形成原电池时,铁作负极 | |
| B. | 形成原电池时,铜作负极 | |
| C. | 形成原电池时,电流由铁经导线流向铜 | |
| D. | 铁铆钉发生了化学腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W、X只能形成一种化合物 | B. | 氧化物的水化物的酸性:Y<Z | ||
| C. | 离子半径:Y>Z>X | D. | X与Y不能存在于同一离子化合物中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com