
常温下,甲组中的某种物质能与乙组中的所有物质发生反应,甲组中的该物质是
甲组 | ①Al(OH)3 ②SiO2 ③ FeCl3溶液 ④ SO2 |
乙组 | a.NaOH溶液 b.浓HNO3 c.氨水 d.氯水 e.H2O2溶液 |
A.① B.② C.③ D.④
科目:高中化学 来源:2015届江苏省中学高三上学期第一次月考化学试卷(解析版) 题型:选择题
在下列各溶液中,离子一定能大量共存的是:
A.pH=11的溶液中:CO32-、Na+、AlO2-、NO3-
B.含有0.1mol·L-1Fe3+的溶液中:K+、Mg2+、I-、NO3-
C.无色溶液中:K+、Na+、MnO4-、SO42-
D.室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源:2015届江苏连云港市高三上第一次月考化学试卷(解析版) 题型:选择题
在某100mL混合酸中,硝酸物质的量浓度为0.4mol/L,硫酸物质的量浓度为0.2mol/L,向其中加入3.2g铜粉,微热,待其充分反应后,溶液中铜离子的物质的量浓度约为
A.0. 15mol/L B.0.3mol/L C.0.5mol/L D.无法计算
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市高三上学期期中考试化学试卷(解析版) 题型:填空题
(14分)磺酰氯(SO2Cl2)是一种有机氯化剂,也是锂电池正极活性物质。已知磺酰氯是一种无色液体,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解。
(1)已知:①SO2 (g) +Cl2 (g)+ SCl2 (g) 2SOCl2 (g) △H=a kJ·mol-1
2SOCl2 (g) △H=a kJ·mol-1
②SO2Cl2(g)+ SCl2 (g)  2SOCl2(g) △H=b kJ·mol-1
2SOCl2(g) △H=b kJ·mol-1
则反应:SO2(g) + Cl2 (g)
(g) SO2Cl2(g) △H = kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K = 。
SO2Cl2(g) △H = kJ·mol-1(用含a、b的代数式表示);该反应平衡常数表达式为K = 。
(2)磺酰氯可与白磷发生反应为:P4 + 10 SO2Cl2 = 4PCl5 + 10SO2↑,若生成1molSO2,则转移电子的物质的量为 mol。
(3)某学习小组的同学依据反应:SO2(g)+ Cl2(g) SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图-1。
SO2Cl2(g) △H <0,设计的制备磺酰氯装置如图-1。

①若用浓盐酸与二氧化锰为原料制取Cl2,其 反应的化学方程式为 。
反应的化学方程式为 。
②有关图-1所示的装置说法正确的是 (不定项选择)。
a.A、E处洗气瓶中盛放的可能分别是饱和食盐水和饱和NaHSO3溶液
b.B处反应管内五球中玻璃棉上的活性炭作催化剂
c.B处反应管冷却水应从m接口通入
d.装置C处吸滤瓶应放在冰水中冷却
e.D处U 形管中盛放的可能是碱石灰
形管中盛放的可能是碱石灰
③从化学平衡移动角度分析,反应管通水冷却的目的为 。
(4)GET公司开发的Li-SO2Cl2军用电池,其示意图如图-2所示,已知电池反应为:2Li + SO2Cl2 = 2LiCl + SO2↑;则电池工作时,正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市高三上学期期中考试化学试卷(解析版) 题型:选择题
25℃时,下列各组离子在指定溶液中一定能大量共存的是
A.能使甲基橙变红的溶液中:Na+、NH4+、MnO4-、SO32-
B.pH=14的溶液中:Mg2+、K+、Cl-、HCO3-
C.0.1mol·L-1 NH4I溶液中:Ca2+、Fe3+、SO42-、Br-
D.0.1mol·L-1 CuCl2溶液中:Mg2+、Al3+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高二上期中化学试卷(必修)(解析版) 题型:选择题
欲将蛋白质从水中析出而又不改变它的性质应加入
A、甲醛溶液 B、饱和Na2SO4溶液 C、CuSO4溶液 D、浓硫酸
查看答案和解析>>
科目:高中化学 来源:2015届河南省原名校高三上学期第一次摸底考试化学试卷(解析版) 题型:填空题
(9分)金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。请完成下列空白:
(1)铝元素在周期表中的位置为________。
(2)在19世纪时,铝是一种珍贵的金属。人们最初得到的铝粒如同珍宝,它的价格同黄金相当。1827 年,德国化学家维勒用金属钾与无水氯化铝反应而制得了金属铝。用钾与无水氯化铝反应制铝而不用氯化铝溶液的理由是_________。现代工业炼铝的原料是由铝土矿提取而得,在提取过程中通入的气体为____。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s) 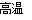 2Al2O3(s)+3Tic(s) △H=-1176kJ/mol。则反应过程中,每转移1 mol电子放出的热量为________。
2Al2O3(s)+3Tic(s) △H=-1176kJ/mol。则反应过程中,每转移1 mol电子放出的热量为________。
(4)硅与铝同周期,地壳里硅铝的含量:硅________铝(填>,<或=)。是硅酸盐玻璃 (Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成Na2O·CaO·6SiO2。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 ________。长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为________。
(5)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:
2Al+4BaO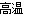 3Ba↑+BaO·Al2O3。利用化学平衡移动原理解释上述方法可制取金属Ba的原因是_____________________________________________________________________________。
3Ba↑+BaO·Al2O3。利用化学平衡移动原理解释上述方法可制取金属Ba的原因是_____________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com