
| A.在已知碱金属元素中它具有最多的电子层数 |
| B.在空气中燃烧时,生成氧化物Fr2O |
| C.氧化物对应的水化物是极强的碱 |
| D.单质的熔点比钠的熔点高 |
科目:高中化学 来源:不详 题型:单选题
| A.元素R能与氧组成RO2化合物 |
| B.化合物RO2在反应中既可作氧化剂也可作还原剂,其化合物不稳定 |
| C.化合物H2R不能燃烧,也不易分解 |
| D.元素R是一种两性元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3种 | B.5种 | C.6种 | D.10 000种 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碱金属 | B.第ⅡA族元素 |
| C.过渡元素 | D.金属与非金属分界线附近的元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
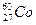 放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。
放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。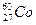 的衰变方程为:
的衰变方程为: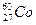 ====
====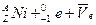
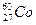 的叙述,错误的是_______________。
的叙述,错误的是_______________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.只有① | B.①②③ |
| C.①③⑤ | D.①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(M-n)∶(m-M) | B.(M-n)∶(m-n) |
| C.(M-m)∶(M-n) | D.(m-n)∶(M-n) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com