

���� ��1�������£�̼�Ͷ������跴Ӧ���ɹ��һ����̼��
��2�������������ݣ����÷����ᴿSiHCl3��
��3�������ɵ���������ˮ��������ŨH2SO4������ȴ�ʹSiHCl3������
��SiHCl3��������Ӧ�й赥�����ɣ����ݹ����ɫ�ж�Dװ���е���ɫ�仯����Ӧ�¶Ƚϸߣ���ͨ������������SiHCl3��H2��Ӧ���ɹ���Ȼ��⣻
�������ǿ�ȼ�����壬�ײ�����ը��Ϊ��ֹ��ȫ�¹ʵķ�����������ͨһ��ʱ��H2����װ���еĿ����ž���
��� �⣺��1�������£�̼�Ͷ������跴Ӧ���ɹ��һ����̼����Ӧ����ʽΪ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����
�ʴ�Ϊ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����
��2��SiHCl3���е�33.0�棩�к�������SiCl4���е�57.6�棩��HCl���е�-84.7�棩�����ڷе���ϴ���ͨ�������ȥ���ʣ�
�ʴ�Ϊ������
��3����п��ϡ����ķ�Ӧ�Ƿ��ȷ�Ӧ���������ɵ���������ˮ������Ϊ����������һ��ѡ��ŨH2SO4�������ķ�Ӧ���ʽϴ����Լ��ȵ�Ŀ����ʹSiHCl3������
�ʴ�Ϊ��Ũ���ʹ������ƿ�е�SiHCl3������
�ڸ����£�SiHCl3��������Ӧ���ɹ赥�ʣ��赥���ǻҺ�ɫ���壬����Dװ���е������ǣ�ʯӢ�ܵ��ڱڸ��лҺ�ɫ���壻��Ӧ����ʽΪ��SiHCl3+H2$\frac{\underline{\;����\;}}{\;}$Si+3HCl��
�ʴ�Ϊ��SiHCl3+H2$\frac{{\underline{1000��1100{\;}^��C}}}{\;}$Si+3HCl��
�������ǿ�ȼ�����壬�����������ﵽһ��ʱ�ײ�����ը��Ϊ��ֹ��ȫ�¹ʵķ�����������ͨһ��ʱ��H2����װ���еĿ����ž���
�ʴ�Ϊ����ͨһ��ʱ��H2����װ���еĿ����ž���
���� ���⿼����ʵ�鷽����Ƶ��й�֪ʶ�������Ӻ��������ӵļ����ڸ߿����г��֣��������͵����Ǹ߿����ȵ㣬��ѧϰ���ص㣬�����ʵ��Ŀ�ĺ����ʵ�����ѡȡʵ��װ�ú�ʵ��ҩƷ��Ȼ�������Ӧ��ʵ�飬��Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2�ͳ���ʯ��ˮ | B�� | NaOH��Һ��CO2 | ||
| C�� | Na2CO3��Һ������ | D�� | NaHCO3��Һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
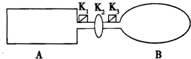 ��ͼװ���У�A���ɵ��Ȳ����Ƴɵ��ܱ�������B���ͻ�ѧ��ʴ�����ڴ��ȵ������ر�K2����������1molNO2ͨ��K1��K3�ֱ��A��B�У���Ӧ��ʼʱ��A��B�������ͬ��Ϊa L����֪��2NO2��g��?N2O4��g����H��0
��ͼװ���У�A���ɵ��Ȳ����Ƴɵ��ܱ�������B���ͻ�ѧ��ʴ�����ڴ��ȵ������ر�K2����������1molNO2ͨ��K1��K3�ֱ��A��B�У���Ӧ��ʼʱ��A��B�������ͬ��Ϊa L����֪��2NO2��g��?N2O4��g����H��0�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����뺣���������γ� | B�� | ���м���ʯ����Ƶö��� | ||
| C�� | FeCl3��Һ���ֻ�ɫ | D�� | ��ͬƷ�Ƶ�īˮ���ܻ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪ˮ��25���95��ʱ�������ƽ��������ͼ��ʾ��
��֪ˮ��25���95��ʱ�������ƽ��������ͼ��ʾ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com