
【题目】短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如下图所示。R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的化合物Z2T能破坏水的电离平衡。下列推断正确的是( )
A.原子半径和离子半径均满足:Y<Z
B.氢化物的沸点不一定是:Y>R
C.最高价氧化物对应水化物的酸性:T<R
D.由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性
【答案】B
【解析】R原子最外层电子数是电子层数的2倍,可能为C或S,由于图示原子半径和原子序数关系可知R应为C;Y与Z能形成Z2Y、Z2Y2型离子化合物,应为Na2O、Na2O2 , 则Y为O,Z为Na;Z与T形成的Z2T化合物能破坏水的电离平衡,T应为S,Na2S水解呈碱性,可促进水的电离;X的原子半径最小,原子序数最小,应为H元素。
A.原子半径O<Na,离子半径O2->Na+ , 故A不符合题意;
B.R为C,对应的氢化物为烃,如含碳原子数较多,常温下为固体,沸点较高,则氢化物的沸点不一定是:Y>R,故B符合题意;
C.非金属性S>C,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故C不符合题意;
D.由H、C、O、Na四种元素组成的化合物不仅仅为NaHCO3 , 可能为有机盐且含有羧基,溶液不一定为碱性,可能为酸性,故D不符合题意;
故选B。R原子最外层电子数是电子层数的2倍,可能为C或S,由于图示原子半径和原子序数关系可知R应为C;Y与Z能形成Z2Y、Z2Y2型离子化合物,应为Na2O、Na2O2 , 则Y为O,Z为Na;Z与T形成的Z2T化合物能破坏水的电离平衡,T应为S,Na2S水解呈碱性,可促进水的电离;X的原子半径最小,原子序数最小,应为H元素,据此解答即可。


科目:高中化学 来源: 题型:
【题目】下列电离方程式正确的是( )
A.盐酸:HCl→H++Cl﹣
B.硫酸:H2SO4→H2++SO42﹣
C.硫酸铝:Al2(SO4)3→Al23++(SO4)32﹣
D.氢氧化钠:NaOH→Na++H++O2﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( ) 
A.①为简单立方堆积②为六方最密堆积③为体心立方堆积④为面心立方最密堆积
B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C.晶胞中原子的配位数分别为:①6,②8,③8,④12
D.空间利用率的大小关系为:①<②<③<④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1表示一些晶体中的某些结构,他们分别是氯化钠、氯化铯、干冰、金刚石、石墨结构中的某一种的某一部分(黑点可表示不同或相同的粒子).
(1)其中代表金刚石的是(填编号字母,下同),金刚石中每个碳原子与个碳原子最接近且距离相等.
(2)其中代表石墨的是 , 其中每个正六边形占有的碳原子数平均为个;
(3)其中表示氯化钠的是 , 每个钠离子周围与它最接近且距离相等的钠离子有个;
(4)代表氯化铯的是 , 每个铯离子与个氯离子紧邻;
(5)代表干冰的是 , 每个二氧化碳分子与个二氧化碳分子紧邻;
(6)由Mg、C、Ni三种元素形成的一种具有超导性的晶体,晶胞如图2所示.Mg位于C和Ni原子紧密堆积所形成的空隙当中.与一个Ni原子距离最近的Ni原子的数目为 , 该晶体的化学式为 . 若该晶体的相对分子质量为M,阿伏加德罗常数为NA , Mg、C、Ni三种元素的原子半径分别为r1pm、r2pm、r3pm,则该晶体的密度表达式为gcm﹣3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)气体制备时须先检查装置的气密性,下列各图所示装置,肯定不符合气密性检查要求的是 .
(Ⅱ)下面是中学化学实验中常见的几种仪器:
a.量筒 b.容量瓶 c.分液漏斗 d.托盘天平 e.温度计
(1)其中标示出仪器使用温度的是 (填编号).
(2)称取10.5g固体样品(1g以下使用游码)时,将样品放在了天平的右盘,则所称样品的实际质量为 g.
(3)使用前要检查仪器是否漏液的是 (填编号).
(Ⅲ)实验室需要95mL 1.0molL﹣1稀硫酸,现用98%的浓硫酸(其密度为1.84g/mL)来进行配制.若实验仪器有:
A.100mL量筒 B.托盘天平 C.玻璃棒 D.250mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
(1)需量取浓硫酸的体积为 mL.
(2)实验时选用的仪器有(填序号)
(3)配制过程中,下列情况会使配制结果偏高的是(填序号)
A.将稀释的硫酸液转移至容量瓶后,未洗涤烧杯和玻璃棒.
B.将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外.
C.未冷却至室温就定容.
D.用胶头滴管加水时,俯视观察溶液凹液面与容量瓶刻度相切.
E.容量瓶使用时未干燥
F.定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.钠和水反应:2Na+2H2O═2Na++2OH﹣+H2↑
B.碳酸钙与稀醋酸的反应:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
C.铜与稀硝酸的反应:Cu+2H+═Cu2++H2↑
D.常温下,用氢氧化钠溶液吸收多余的氯气:Cl2+OH﹣═Cl﹣+ClO﹣+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物C是一种医药中间体,可通过下列方法合成:
(1)A中含氧官能团的名称为和 .
(2)B的结构简式为 .
(3)B→C的反应类型为 .
(4)C的同分异构体D能发生银镜反应,能与FeCl3溶液发生显色反应,且1molD最多能与2molNaOH反应.D分子中有4种不同化学环境的氢.请写出D的一种结构简式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
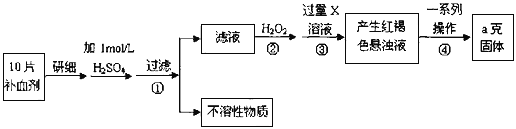
请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有__________________(填离子符号),检验滤液中还存在Fe2+的方法为_________________________________________。(注明试剂、现象)
(2)步骤②加入过量H2O2的目的:____________________________________________。
(3)步骤③中反应的离子方程式:_____________________________________________。
(4)若实验无损耗,则每片补血剂含铁元素的质量__________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com