
| 催化剂 |
| 加热 |
| ||
| △ |
| ||
| 10min |


 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:
| D |
| E |
| D |
| E |
查看答案和解析>>
科目:高中化学 来源: 题型:
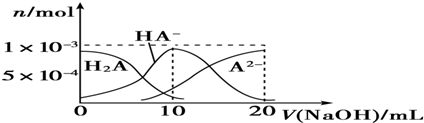
| A、H2A是二元弱酸 |
| B、当0 mL<V(NaOH)<20 mL时,一定有:c(OH-)+c(HA-)+2c(A2-)=c(Na+)+c(H+) |
| C、当V(NaOH)=10 mL时,溶液中离子浓度关系一定有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| D、当V(NaOH)=20 mL后,再向溶液中加水稀释,c(H+)减小,c(OH-)也减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 序号 | 实验内容 | 实验结果 |
| 1 | 加AgNO3溶液 | 有白色沉淀生成 |
| 2 | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
| 3 | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.63g,第二次称量读数为4.66g |
| 阴离子符号 | 物质的量浓度(mol/L) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1的溶液中:Na+、Mg2+、SO42-、HCO3- |
| B、含有大量Fe3+的溶液中:.Al3+、Cu2+、Cl-、SO42- |
| C、加入Al能放出H2的溶液中:K+、NH4+、NO3-、Cl- |
| D、使蓝色石蕊试纸变红的溶液:K+、S2-、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、若生成7.1 g Cl2,则转移0.1 mol电子 |
| B、MnO2是氧化剂 |
| C、HCl是还原剂 |
| D、该反应是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
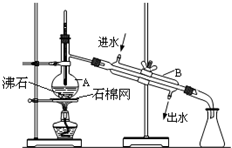 如图为实验室分离水和乙醇的装置图,根据图示回答下列问题.
如图为实验室分离水和乙醇的装置图,根据图示回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com