
【题目】用乙烯、甲苯、E三种原料合成高分子药物M和有机中间体L的路线如图: 
已知: 
Ⅲ.有机物L是一种六元环酯,M的分子式是(C15H16O6)n
(1)C中含氧官能团的名称 , D的结构简式
(2)E在KMO4/OH﹣中转化成F,F的结构简式 , H→J的反应类型 .
(3)H→L的化学反应方程式是 .
(4)K→M属于加聚反应,K的结构简式是 .
(5)写出一定量的C与足量NaOH溶液反应的化学方程式 .
(6)写出一种符合下列条件的C的同分异构体的结构简式 .
①属于芳香族化合物;
②能发生银镜反应;
③遇FeCl3溶液能发生显色反应
④核磁共振氢谱有4组峰,且峰面积之比为l:l:2:2.
【答案】
(1)羟基、羧基;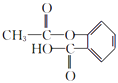
(2)![]() ;消去反应
;消去反应
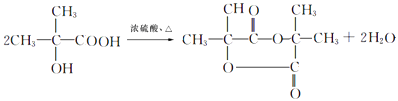
(3)
(4)
(5)![]()
(6) 或
或 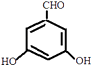 或
或 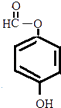
【解析】解:由反应信息Ⅰ可知,乙烯在高锰酸钾、碱性条件下被氧化生成B为HOCH2CH2OH.由反应信息Ⅱ可知, ![]() 与乙酸酐反应生成D为
与乙酸酐反应生成D为 ![]() .F发生催化氧化生成G,G与形成氢氧化铜反应生成H,则F为醇、G含有醛基、H含有羧基,L是六元环酯,由H、L的分子式可知,应是2分子H脱去2分子水发生酯化反应,故H中还含有﹣OH,且﹣OH、﹣COOH连接在同一碳原子上,该碳原子不含H原子,故H为
.F发生催化氧化生成G,G与形成氢氧化铜反应生成H,则F为醇、G含有醛基、H含有羧基,L是六元环酯,由H、L的分子式可知,应是2分子H脱去2分子水发生酯化反应,故H中还含有﹣OH,且﹣OH、﹣COOH连接在同一碳原子上,该碳原子不含H原子,故H为  ,逆推可得G为
,逆推可得G为  、F为
、F为 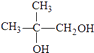 ,故E为(CH3)2C=CH2 , 在高锰酸钾、碱性条件下氧化生成F.B、D、J反应生成K,K→M属于加聚反应,M分子式是(Cl5Hl6O6)n , 由M的链节组成可知,应是1分子B、1分子D、1分子J反应生成K,故H在浓硫酸、加热条件下发生消去反应生成J为CH2=C(CH3)COOH,K为
,故E为(CH3)2C=CH2 , 在高锰酸钾、碱性条件下氧化生成F.B、D、J反应生成K,K→M属于加聚反应,M分子式是(Cl5Hl6O6)n , 由M的链节组成可知,应是1分子B、1分子D、1分子J反应生成K,故H在浓硫酸、加热条件下发生消去反应生成J为CH2=C(CH3)COOH,K为  、M为
、M为 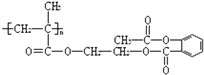 ,(1)由C的结构简式可知,C中含氧官能团的名称为羟基、羧基,D为
,(1)由C的结构简式可知,C中含氧官能团的名称为羟基、羧基,D为 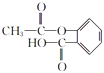 ,所以答案是:羟基、羧基;
,所以答案是:羟基、羧基;  ;(2)根据上面的分析可知,F为
;(2)根据上面的分析可知,F为 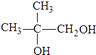 ,H→J的反应类型消去反应,
,H→J的反应类型消去反应,
所以答案是: 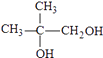 ;消去反应;(3)H→L的化学反应方程式是
;消去反应;(3)H→L的化学反应方程式是 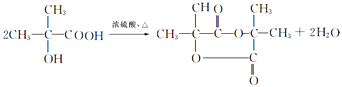 ,
,
所以答案是: 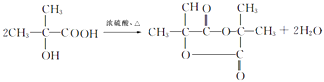 ;(4)根据上面的分析可知,K的结构简式是
;(4)根据上面的分析可知,K的结构简式是 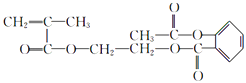 ,
,
所以答案是:  ;(5)一定量的C与足量NaOH溶液反应的化学方程式为
;(5)一定量的C与足量NaOH溶液反应的化学方程式为 ![]() ,
,
所以答案是: ![]() ;(6)符合下列条件的C(
;(6)符合下列条件的C( ![]() )的同分异构体:
)的同分异构体:
①属于芳香族化合物,含有苯环;②能发生银镜反应,含有﹣CHO或﹣OOCH,若为﹣CHO,则还含有2个﹣OH,若为﹣OOCH,则还含有1个﹣OH.③核磁共振氢谱有4组峰,且峰面积之比为1:1:2:2,符合条件的同分异构体为: 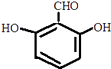 、
、 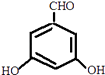 、
、  ,
,
所以答案是:  或
或  或
或 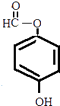 .
.


科目:高中化学 来源: 题型:
【题目】下列叙述中错误的是( )
A. H2SO4的摩尔质量是98
B. 2mol NO和2mol N2含分子数相同
C. 1mol Cl2的质量是71g
D. 标准状况下1mol O2与1mol H2气体所占的体积都约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是信息高速公路的基石,通常以硅石(SiO2>99.0%、还有少量的Al2O3、Fe2O3等)为主要原料制备,主要流程如图所示. 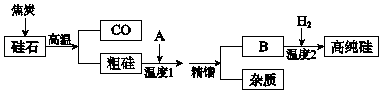
(1)从硅石中得到粗硅的化学方程式是 , 粗硅含有的杂质有铝、等.
(2)二氧化硅与焦炭在高温下也能得到一种硬度仅次于金刚石的物质金刚砂(化学式为SiC,Si为+4价),原理是SiO2+3C ![]() SiC+2CO↑,该反应中的氧化剂是 .
SiC+2CO↑,该反应中的氧化剂是 .
(3)若A是氯气,B是四氯化硅,精馏得到纯净SiCl4 , 温度应控制的范围是(填序号).
物质 | SiCl4 | SiHCl3 | FeCl3 | AlCl3 |
熔点/℃ | ﹣70 | ﹣128.2 | 306 | ﹣﹣ |
沸点/℃ | 57.6 | 31.85 | 315 | 181 升华 |
a.55~60℃b.180~200℃c.300~320℃
则精馏分离出的杂质成分是 .
(4)若A是HCl,B是SiHCl3 , 生产过程中可循环利用的物质是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛合金烤瓷牙是目前国内使用最为普遍的一种烤瓷牙,TiCl4是生产金属钛的原料.
(1)工业上主要用TiO2氯化的方法来制取TiCl4
①有人拟用以下氯化反应来制取TiCl4:TiO2(s)+2Cl2(g)TiCl4(l)+O2(g),写出实验室用二氧化锰与浓盐酸反应制取Cl2的离子方程式 .
②工业上通常往TiO2和Cl2反应体系中加入碳单质,在一定条件下制取TiCl4 , 从化学平衡的角度解释此方法能顺利制取TiCl4的原因 .
(2)某化学实验小组以TiO2和足量 CCl4为原料制取TiCl4 , 装置如图1所示: 
如表是有关物质的性质:
物质 | 熔点/℃ | 沸点/℃ | 其他 |
CCl4 | ﹣23 | 76.8 | 与TiCl4互溶 |
TiCl4 | ﹣25 | 136 | 遇潮湿空气产生白雾 |
①实验开始时先点燃A处的酒精灯,待C中烧瓶里有液滴出现时再点燃B处的酒精灯,其主要目的是 .
②本实验中仪器a采用题给的加热方式的突出优点是 .
③B中CCl4与TiO2发生反应的化学方程式是 .
④欲分离C装置中的TiCl4 , 应采用的实验操作为(填操作名称).
⑤若将反应过程中生成的气体X(足量)缓缓通入Ba( OH)2和NaOH的混合稀溶液中,生成沉淀的物质的量(n)和 通入气体X的体积(V)的关系如图2所示,若混合溶液中Ba( OH)2和2NaOH的物质的量之比为1:1,则b点溶液中溶质主要成分的化学式为 , 从b点到c点,沉淀减少过程中发生反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)羟基的电子式
(2)相对分子质量为72且沸点最高的烷烃的结构简式为
(3)写出方程式:实验室制乙炔 .
(4)写出: ![]() 形成六元环酯的结构简式
形成六元环酯的结构简式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乙醇和乙二醇互为同系物
B.异丙苯( ![]() )分子中碳原子可能都处于同一平面
)分子中碳原子可能都处于同一平面
C.按系统命名法,化合物( ![]() )的名称是2,3,5,5一四甲基一4,4一二乙基己烷
)的名称是2,3,5,5一四甲基一4,4一二乙基己烷
D.![]() 的一溴代物和
的一溴代物和 ![]() 的一溴代物都有4种(不考虑立体异构)
的一溴代物都有4种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于氧化还原反应的是( )
A.CaO+H2O═Ca(OH)2
B.CH4+2O2 ![]() 2H2O+CO2
2H2O+CO2
C.CaCO3 ![]() CaO+CO2↑
CaO+CO2↑
D.Na2SiO3+2HCl═2NaCl+H2SiO3(胶体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化石燃料的燃烧会产生大量污染大气的二氧化硫和温室气体二氧化碳.而氢气和氨气都被认为是无碳无污染的清洁能源. 
(1)某些合金可用于储存于氢,金属储氢的原理克表示为M+xH2═MH2x(M表示某种合金).如图1表示温度分别为T1、T2且T1<T2时最大吸氢量与氢气压强的关系.则该反应的△H0(填“>”或“<”)
(2)氨在氧气中燃烧,生成水和一种空气组成成分的单质.已知:N2(g)+3H2(g)2NH3(g)△H=﹣92KJmol﹣1及H2的燃烧热为286kJmol﹣1;试写出氨在氧气中燃烧生成液态水的热化学方程式: .
(3)在一定条件下,将1molN2和3molH2混合与一个10L的容积不变的密闭容器中发生反应,5分钟后达到平衡,平衡时氨的体积分数为25%.
①反应的平衡常数表达式为;
②反应开始到平衡时H2的消耗速率v(H2)=;
③能判断该反应是否达到化学平衡状态的依据是;
a 容器中压强不变 b.混合气体的密度不变
c.3v(H2)=2v(NH3) d.c(N2):c(H2):c(NH3)=1:3:2
④对于上述平衡状态,改变下列条件能使反应速率增大,且平衡向正向移动的是;
a 选用更高效的催化剂 b 升高温度c 及时分离出氨气 d 增加H2的浓度
⑤如今采用SCY陶瓷固体电解质的电化学合成氨装置(如图2),该装置用可以传导质子的固态物质作为介质.电池总反应为N2(g)+3H2(g)2NH3(g),那么该电解池阴极反应式为 , 当阳极失去0.6mol电子时,阴极产生的气体在标准状态下的体积为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长式周期表共有18个纵行,从左到右排为1—18列,即碱金属为第一列,稀有气体元素为第18列。按这种规定,下列说法正确的是 ( )
A.s区元素都是金属元素B.第13列的元素原子最外层电子排布为ns2 np1
C.第四周期第9列元素是铁元素D.第10、11列为ds区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com