
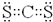 ,ci2与ce2比较,沸点较高的是CS2(写分子式).
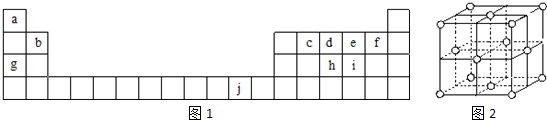
,ci2与ce2比较,沸点较高的是CS2(写分子式).分析 根元素在周期表中的位置可知a~j分别是H、Be、C、N、O、F、Na、P、S、Cu.
(1)f是F元素,F元素原子核外有9个电子,构造原理书写基态F原子核外电子排布式;
(2)该分子是苯,苯是平面正六边形结构,每个C原子价层电子对个数是3且不含孤电子对,根据价层电子对互斥理论判断C原子杂化方式;分子中正负电荷重心重合的分子为非极性分子;
(3)CS2是由极性键构成的非极性分子,电子式为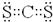 ,CO2和CS2都是分子晶体,分子晶体熔沸点与分子间作用力成正比;
,CO2和CS2都是分子晶体,分子晶体熔沸点与分子间作用力成正比;
(4)同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电离能大于其相邻元素;同一周期元素,元素电负性随着原子序数增大而增大;
(5)A.J是铜,位于第四周期第IB族;
B.d是N元素,氮元素的2p属于半充满,属于p区;
C.最外层电子排布式为4s1,该元素不一定位于第IA族;
D.最外层电子排布式为ns2np1,该元素位于ⅢA族;
(6)氨气和铜离子可形成配位键,氢氧化铜和一水合氨反应生成铜氨络合离子;
(7)利用均摊法计算该晶胞中原子个数,从而确定化学式.
解答 解:根元素在周期表中的位置可知a~j分别是H、Be、C、N、O、F、Na、P、S、Cu.
(1)f是F元素,F元素原子核外有9个电子,构造原理书写基态F原子核外电子排布式为1s22s22p5,
故答案为:1s22s22p5;
(2)该分子是苯,苯分子中每个C原子价层电子对个数是4且不含孤电子对,则C原子杂化方式为sp2,该分子正负电荷重心重合,所以属于非极性分子,故答案为:sp2;非极性分子;
(3)CS2是由极性键构成的非极性分子,电子式为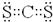 ;CO2和CS2都是分子晶体,沸点高低和分子间作用力大小有关系,由于相对分子质量是CS2的大,所以的CS2沸点高,
;CO2和CS2都是分子晶体,沸点高低和分子间作用力大小有关系,由于相对分子质量是CS2的大,所以的CS2沸点高,
故答案为: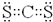 ;CS2;
;CS2;
(4)由于磷原子的3p轨道属于半充满,稳定性好,因此第一电离能大于S的;金属性越弱,电负性越小,所以钠的电负性小于Be的,故答案为:>;<;
(5)A.J是铜,位于第四周期第IB族,故正确;
B.d是N元素,氮元素的2p属于半充满,属于p区,故B正确;
C.最外层电子排布式为4s1,该元素不一定位于第IA族,如铜的最外层电子排布式为4s1,但铜属于第IB,故错误;
D.最外层电子排布式为ns2np1,该元素位于ⅢA族,故错误;
故选AB;
(6)氨气和铜离子可形成配位键,所以氢氧化铜和一水合氨反应生成蓝色的[Cu(NH3)4]2+,该反应离子方程式为Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O,故答案为:[Cu(NH3)4]2+;
(7)根据晶胞结构图可知,含有的铜原子是8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,故答案为:4.
点评 本题考查物质结构和性质及元素周期表,为高频考点,涉及晶胞计算、配合物、元素周期律、原子核外电子排布等知识点,明确物质结构、物质性质、元素周期表结构是解本题关键,难点是铜氨络合离子的书写,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子半径D>E>C>B | |
| B. | A、C、D、E四种元素形成的化合物溶于水一定显酸性 | |
| C. | C、D形成的化合物是离子化合物,只含有离子键 | |
| D. | A、C形成的化合物只有氧化性没有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是指常温常压下,2个氢分子和1个氧分子反应生成2个水分子,放出热量571.6 kJ | |
| B. | 是指常温常压下,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),放出热量571.6 kJ | |
| C. | 是指标准状况下,2 mol H2O(l)分解为2 mol H2(g)和1 mol O2(g),吸收热量571.6 kJ | |
| D. | 是指常温常压下,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),放出热量571.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用浓硫酸干燥H2、NH3、Cl2等气体 | |
| B. | 向某溶液中加入BaCl2溶液出现白色沉淀,则该溶液中肯定有SO42- | |
| C. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 | |
| D. | 氨水、铵盐受热都易发生化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 、C
、C .反应④所用试剂和条件是氢氧化钠醇溶液、加热.
.反应④所用试剂和条件是氢氧化钠醇溶液、加热. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应及 离子方程式 | 评 价 |
| A | 醋酸钠溶于水:CH3COO-+H2O═CH3COOH+OH- | 正确 |
| B | 实验室用浓盐酸与MnO2反应制Cl2: MnO2+4H++2Cl- $\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O | 错误,反应物中HCl电离出的H+、Cl-比例为1:1 |
| C | 硝酸铁溶液中加过量氨水:Fe3++3NH3•H2O═Fe(OH)3(胶体)+3NH4+ | 错误,Fe(OH)3应该是沉淀 |
| D | 铝溶于碳酸中:2Al+3H2CO3═2Al3++3H2+3 CO32- | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
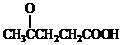 )合成聚芳酯E的路线:
)合成聚芳酯E的路线: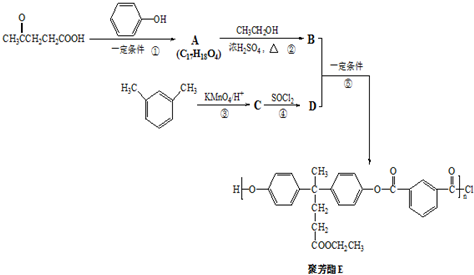
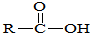 →
→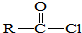 +SO2+HCl
+SO2+HCl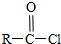 +R′OH→
+R′OH→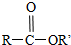 +HCl(R、R′表示烃基)
+HCl(R、R′表示烃基)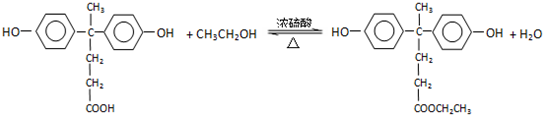 .
.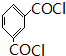 .
.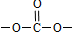 结构 ④苯环上只有2个取代基在上述同分异构体中,写出其中任一种与足量NaOH溶液共热反应的化学方式:
结构 ④苯环上只有2个取代基在上述同分异构体中,写出其中任一种与足量NaOH溶液共热反应的化学方式: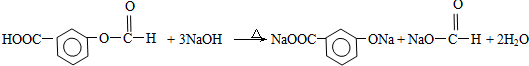 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com