
A.、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)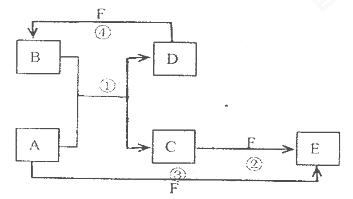
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电予数D是A的2倍,F的浓溶液与A D反应都有红棕色气体生成,则A为___________________,
反应④的化学方程式为____________________________________.
(2)若A为常见的金属单质,D F是气态单质,反应①在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是____________________________.
(3)若A.D.F都是短周期非金属元素单质,且A.D所含元素同主族,A.F所含元素同周期,则反应①的化学方程式为________________________.
(1)Mg;C+4HNO3(浓)= CO2↑+4NO2↑+2H2O;
(2)2Fe2++Cl2=2Fe3++2Cl-
(3)2C+SiO2 2CO↑+Si
2CO↑+Si
解析试题分析:(1)原子序数A是D的2倍,则A的原子序数是偶数;最外层电子数D是A的2倍,则D的最外层电子数是偶数,在短周期的偶数主族中,只有Mg与C符合题意,所以A是Mg,D是C。则B是CO2,F的浓溶液与A D反应都有红棕色气体生成,红棕色气体是二氧化氮,F是硝酸。反应④是C与浓硝酸的反应,化学方程式为C+4HNO3(浓)= CO2↑+4NO2↑+2H2O;
(2)A为常见的金属单质,根据反应流程特点,判断A是铁,F是氯气,D是氢气,则B是盐酸,C是氯化亚铁,氯化亚铁与氯气反应生成氯化铁,所以反应②的离子方程式为2Fe2++Cl2=2Fe3++2Cl-
(3)同主族元素之间的置换反应有C与Si,O与S,H与Na,卤族元素之间的置换,代入题目可知C与Si符合题意,则A是C,D是Si,则C是CO,C与CO都与氧气反应生成二氧化碳,所以F是氧气。反应①是制取粗硅的反应,化学方程式为2C+SiO2 2CO↑+Si。
2CO↑+Si。
考点:考查元素的推断,根据反应特点推断元素的种类,单质之间的置换反应的判断,化学方程式的书写


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:单选题
下列关于金属性质的叙述中正确的是
| A.钠与氧气反应时,产物是由O2的用量决定的 |
| B.铝箔在空气中受热可以熔化且会发生剧烈燃烧 |
| C.金属与非金属发生反应时,被氧化的一定是金属 |
| D.铁丝不论在空气中还是纯氧中都不会燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列化学实验事实及其解释不正确的是
| A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3 |
| B.钠保存在煤油中,是因为煤油不与钠反应,且钠比煤油密度大、煤油可以隔绝空气 |
| C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 |
| D.钠长期暴露在空气中的产物是Na2CO3,原因是钠在空气中生成的Na2O会与水和二氧化碳反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分) 现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。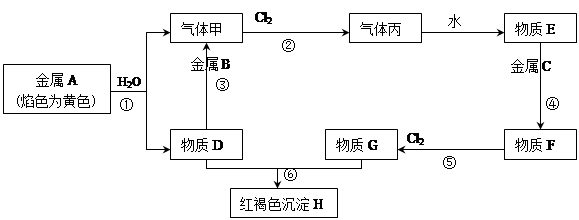
请回答下列问题:
(1)写出下列物质的化学式:B 、丙
(2)写出下列反应的化学方程式:
反应① ;反应③ ;
反应⑥ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
化合物甲是由短周期元素组成的陶瓷材料,是一种以共价键相连的物质,具有耐高温、抗冲击、导热性好等优良性质。乙是制备这种材料的起始原料,也是铝土矿的主要成分。制备时采取碳热还原氮化法,即把乙与炭粉按一定比例混合,在流动N2气氛中加热到一定温度即可得到甲和可燃性气体丙,二者原子个数之比均为1:1。8.2g甲与足量的氢氧化钠溶液混合可以得到无色溶液丁,并产生标准状况下4.48L气体戊。
(1)乙的化学式为 ,写出它的一种用途 。
(2)甲的晶体类型为 ,写出碳热还原氮化法制甲的化学方程式 。
(3)工业制备甲的过程中可能含有的杂质有 。
(4)气体戊的结构式为 ,写出甲与足量的氢氧化钠溶液反应的化学方程式为 ,验证溶液丁中溶质的实验方法为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如图所示(部分反应中的H2O已略去)。请按要求回答下列问题:
(1)若D为金属单质,且D是用量最大、用途最广的金属,若加热蒸干B的溶液没有得到B的盐,则B的化学式可能为__________________________。
(2)若A常用作制冷剂,B和D为空气的主要成分,则反应(Ⅲ) 的化学方程式为______________。
(3)若D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式可以是_________________________。
(4)若D为酸或酸性气体,则A、B、C、D可以是________________(请按顺序写出合理的答案)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(8分)将稀硝酸逐滴加入盛有铝铁合金的容器中,当固体恰好完全溶解时,产生标准状况下NO 40.32L,将反应后的溶液平均分成三等份,分别进行如下实验:
(1)第一份溶液中逐滴加入2 mol·L-1NaOH溶液,至恰好达到最大沉淀,不考虑空气中O2的氧化,则需加入NaOH溶液的体积为________________。
(2)第二份溶液中边加入NaOH溶液,边在空气中充分搅拌,至恰好达到最大沉淀量,将产生的沉淀过滤、洗涤、干燥、称量比第一份重5.1g,则该过程中消耗O2的物质的量为_______________。
(3)第三份溶液中逐滴加入4 mol·L-1NaOH溶液,至Al(OH)3沉淀恰好溶解,消耗NaOH溶液500mL,计算原合金中铝的质量。(写出解题过程)(4分)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
我国化工专家侯德榜,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。生产流程如下: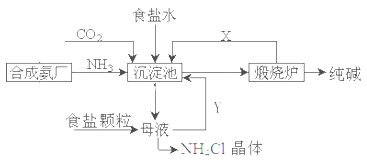
(1)完成有关反应的化学方程式
①沉淀池: NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl
②煅烧炉:
(2)联合制碱法的优点表述中,不正确的是___________
A.生产原料为:食盐、NH3、CO2
B.副产物氯化铵可做氮肥
C.生产过程中可循环利用的物质只有CO2
D.原料利用率高
某实验小组,利用下列装置模拟“联合制碱法”的第一步反应。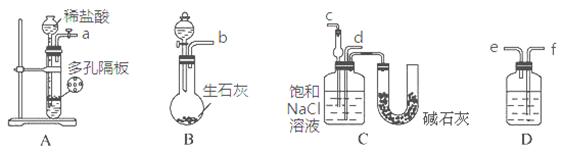
(3)上述装置中接口连接顺序为 ;
A.a接c;b接f、e接d B.a接d;b接f、e接c
C.b接d;a接e、f接c D.b接c;a接f、e接d
(4)D中应选用的液体为 。
为测定产品纯碱的成分和含量,做如下实验。假设产品纯碱中只含NaCl、NaHCO3杂质。
(5)检验产品纯碱中是否含有NaCl,可取少量试样溶于水后,再滴加 试剂。
(6)滴定法测定纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用c mol/L的HCl溶液滴定至溶液由红色变为无色(指示CO32- +H+=HCO3-反应的终点),所用HCl溶液体积为V1 mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄色变为橙色,所用HCl溶液总体积为V2 mL。则纯碱样品中NaHCO3质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式: ,反应后得到的溶液呈 色。用此溶液分别做如下实验:
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为 ,此反应属于 (填反应类型)。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈 色,即制得Fe(OH)3胶体。
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到 烧杯中的液体产生丁达尔效应。这个实验可以用来区别 。
(4)用Fe(OH)3胶体进行下列实验:
①将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,这说明 ,这种现象称为 。
②向其中加入饱和(NH4)2SO4溶液发生的现象是 ,原因是 。
③向其中滴入过量稀硫酸,现象是 ,其原因是 。
④提纯此分散系常用的方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com