
【题目】下列有关实验的描述正确的是
A. 加热蒸发皿和烧杯必须垫石棉网
B. 用NaOH溶液滴定醋酸溶液,加入甲基橙作指示剂
C. 将硫酸铜溶液蒸发浓缩、冷却结晶得到CuSO4·5H2O
D. 将一定质量的AlCl3加入到容量瓶中加水定容,配制一定浓度的AlCl3溶液
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X,可能含有Al3+、Ba2+、NH4+ 、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,其现象及转化如下图。有一种气体是红棕色。请回答下列问题:
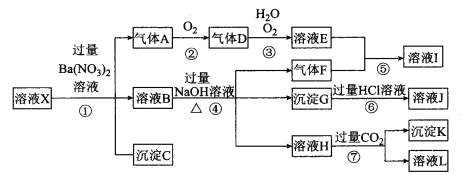
(1)溶液X中除了H+一定存在的离子有________________ 。溶液X中一定不存在的离子有____________ 。
(2)产生气体A的离子方程式为________________________________。
(3)转化⑥发生反应的现象为__________________________________。
(4)转化⑦中的离子方程式为___________________________________。
(5)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,则反应中O2与D的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列相关家庭实验能达到预期目的的是 ( )
相关实验 | 预期目的 | |
A. | 在少量食用碱中一次性加入过量食醋 | 探究食用碱是碳酸钠还是碳酸氢钠 |
B. | 在食用盐中滴加少量淀粉液 | 探究食用盐是否为加碘盐 |
C. | 用激光笔照射淀粉液 | 探究淀粉液是胶体还是溶液 |
D | 将鸡蛋白溶于水后,滴加AgNO3溶液 | 验证蛋白质中含有氯元素 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是( )

A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为Cu2++2e-=Cu
C.无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
D.a和b分别连接直流电流正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氢氟酸在水溶液中建立如下电离平衡:HF ![]() H++F-,如只改变一个条件一定可以使c(HF)/c(H+)减小的是( )
H++F-,如只改变一个条件一定可以使c(HF)/c(H+)减小的是( )
A.通HCl(g) B.加入少量KF(s)
C.加入少NaOH(s) D.通入少量HF(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20.0g质量分数为14.0%的KNO3溶液跟30.0g质量分数为24.0%的KNO3溶液混合,得到的密度为1.15g·cm-3的混合溶液。计算:
(1)混合后溶液的质量分数。
(2)混合后溶液的物质的量浓度。
(3)在1000g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.有A、B、C、D四种化合物,分别由K+、Ba2+、SO42-、CO32-、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断B的化学式。_______________
(2)写出下列反应的离子方程式。
B与盐酸反应:____________________
E(少量)与澄清石灰水反应:___________________
Ⅱ.某气体的分子为双原子分子, 其摩尔质量为Mg/mol,现有标准状况下VL该气体,设阿伏加德罗常数为NA,则
(1)①该气体的物质的量为____________mol;
②该气体在标准状况下的密度为___________g·L-1;
(2)气体化合物A分子式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中充入一定量的N02,发生反应2N02(g)![]() N204(g) △H=一57kJ·mol—1。在温度为T1、T2时,平衡体系中N02的体积分数随压强变化的曲线如图所示。下列说法正确的是 ( )
N204(g) △H=一57kJ·mol—1。在温度为T1、T2时,平衡体系中N02的体积分数随压强变化的曲线如图所示。下列说法正确的是 ( )
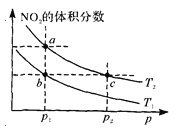
A.a、c两点的反应速率:a>c
B.a、b两点N02的转化率:a<b
C.a、c两点气体的颜色:a深,c浅
D.由a点到b点,可以用加热的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二猛(Mn2O3)在现代工业上应用广泛。以软锰矿(主要成分为MnO2)和硫锰矿(主要成分为MnS)为原料制备高纯度硫酸锰进而制备三氧化二锰的工艺流程如下(两种矿物中均不存在单质杂质):
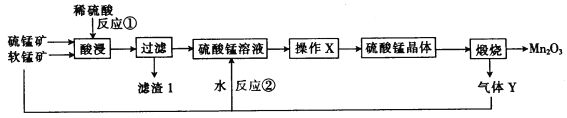
(1)滤渣1中存在一种非金属单质,则“酸浸”时反应①的化学方程式为___________。
(2)操作X为蒸发浓缩、_____________、洗涤烘干。经操作X之后得到MnSO4 H2O。在洗涤操作中,常用酒精洗涤MnSO4 H2O晶体,主要目的是_________________。
(3) 气体Y直接排放会污染空气,将Y的水溶液与软锰矿反应可得硫酸锰,反应②的化学方程式为____________。
(4) Mn2O3与MnO2类似,也能与浓盐酸反应,其反应的离子方程式为___________。
(5)用标准的BaCl2溶液测定样品中MnSO4 H2O的质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略),其原因可能是__________(任写一点)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com