
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成下图所示的原电池。下列判断不正确的是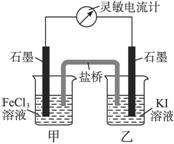

A.为证明反应的发生,可取甲中溶液加入酸性高锰酸钾溶液 |
B.反应开始时,甲中石墨电极上Fe3+被还原,乙中石墨电极上发生氧化反应 |
C.电流计读数为零时,在甲中加入FeCl2固体后,甲中石墨电极为负极 |
| D.此反应正反应方向若为放热反应,电流计读数为零时,降低温度后,乙中石墨电极为负极 |
A
解析试题分析:根据常温下能自动发生的氧化还原反应都可设计成原电池,再利用正反应2Fe3++2I 2Fe2++I2可知,铁元素的化合价降低,而碘元素的化合价升高,则图中甲烧杯中的石墨作正极,乙烧杯中的石墨作负极,利用负极发生氧化反应,正极发生还原反应,并利用平衡移动来分析解答。A、甲中溶液中含有氯离子,也能被酸性高锰酸钾溶液氧化二褪色,故A不正确;B、因乙中I-失去电子放电,元素的化合价升高,发生氧化反应,乙中石墨电极上发生的电极反应式为:2I--2e-═I2,由总反应方程式知,Fe3+被还原成Fe2+,则发生还原反应,故B正确;C、当加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,作为负极,而乙中石墨成为正极,故C正确;D、此反应正反应方向若为放热反应,电流计读数为零时,降低温度后,平衡向正反应方向移动,则乙中石墨电极为负极,故D正确;故选A。
2Fe2++I2可知,铁元素的化合价降低,而碘元素的化合价升高,则图中甲烧杯中的石墨作正极,乙烧杯中的石墨作负极,利用负极发生氧化反应,正极发生还原反应,并利用平衡移动来分析解答。A、甲中溶液中含有氯离子,也能被酸性高锰酸钾溶液氧化二褪色,故A不正确;B、因乙中I-失去电子放电,元素的化合价升高,发生氧化反应,乙中石墨电极上发生的电极反应式为:2I--2e-═I2,由总反应方程式知,Fe3+被还原成Fe2+,则发生还原反应,故B正确;C、当加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,作为负极,而乙中石墨成为正极,故C正确;D、此反应正反应方向若为放热反应,电流计读数为零时,降低温度后,平衡向正反应方向移动,则乙中石墨电极为负极,故D正确;故选A。
考点:考查原电池原理的应用与判断


科目:高中化学 来源: 题型:单选题
燃料电池是燃料(例如CO,H2,CH4等)跟氧气或空气起反应,将此反应的化学能转变为电能的装置,电解质通常是KOH溶液。下列关于甲烷燃料电池的说法不正确的是
| A.负极反应式为CH4+10OH--8e=CO32-+7H2O |
| B.正极反应式为O2+2H2O+4e=4OH- |
| C.随着不断放电,电解质溶液碱性不变 |
| D.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用质量均为100g的铜作电极,电解硝酸银溶液(足量),电解一段时间后,两电极的质量差为28g,此时两电极的质量分别为( )
| A.阳极100g,阴极128g | B.阳极93.6g,阴极121.6g |
| C.阳极91.0g,阴极119.0g | D.阳极86.0g,阴极114.0g |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是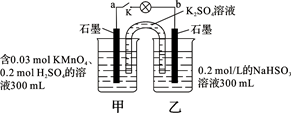
| A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1 |
| B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a |
| C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小 |
| D.乙池中的氧化产物为SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电池的说法不正确的是( )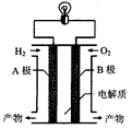
| A.A电极是负极 |
| B.外电路中电子由B电极通过导线流向A电极 |
| C.产物为无污染的水,属于环境友好电池 |
| D.该电池的总反应:2H2+O2===2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在充电过程中的总反应方程式是:
Ni(OH)2 + M =" NiOOH" + MH
已知:6NiOOH + NH3 + H2O + OH-="6" Ni(OH)2 + NO2-
下列说法正确的是
NiMH 电池放电过程中,正极的电极反应式为:NiOOH + H2O + e-= Ni(OH)2 + OH-
充电过程中OH-离子从阳极向阴极迁移
充电过程中阴极的电极反应式:H2O + M + e-=" MH" + OH-,H2O中的H被M还原
D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成甲烷燃料电池。已知通入甲烷的一极,其电极反应为CH4+10OH—-8e- CO32—+7H2O,下列叙述正确的是
CO32—+7H2O,下列叙述正确的是
| A.通入甲烷的一极为正极 |
| B.通入氧气的一极发生氧化反应 |
| C.该电池在工作时,溶液中的阴离子向正极移动 |
D.该电池总反应为CH4+2O2+2OH— CO32— +3H2O CO32— +3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中正确的是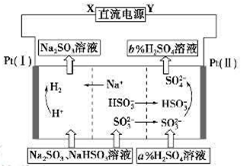
| A.X为直流电源的正极,Y为直流电源的负极 |
| B.阳极区pH减小 |
| C.图中的b<a |
| D.阴极的电极反应为HSO3——2e—+H2O=SO42—+3H+和 SO32——2e—+2H2O=SO42—+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是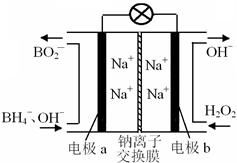
| A.电池放电时Na+从b极区移向a极区 |
| B.电极b采用MnO2,MnO2既作电极材料又有催化作用 |
| C.该电池的负极反应为:BH4-+ 8OH-+8e-→BO2-+ 6H2O |
| D.每消耗3 mol H2O2,转移的电子为3 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com