
【题目】摩拜单车利用车篮处的太阳能电池板向智能锁中的锂离子电池充电,电池反应原理为LiCoO2 +6C![]() li1-xCoO2 +lixC6,结构如图所示。下列说法正确的是
li1-xCoO2 +lixC6,结构如图所示。下列说法正确的是
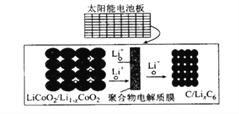
A. 放电时,正极质量增加
B. 充电时,锂离子由右向左移动
C. 该钾离了电池工作时,涉及到的能量形式有3 种
D. 充电时、阳极的电极反应式为Li1-xCoO2+xLi++xe-= LiCoO2
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
【题目】有机物G是一种常见的食用香料。实验室由链状二烯烃A制备G的合成路线如下:

回答下列问题:
(1)A的结构简式为_______,D的化学名称是_______。
(2)③的反应方程式为_______。
(3)④的反应试剂和反应条件分别是_______,⑤的反应类型是_______。
(4)F中官能团名称为_______,G的分子式为_______。
(5)H是E的同分异构体,其分子中含有苯环,苯环上只有2个取代基且处于对位,遇氯化铁溶液显紫色,则H可能的结构有_______种。
(6)已知:①反应物分子的环外双键比环内双键更容易被氧化;
②RHC=CHR RCHO+RCHO(R、R代表烃基或氢原子)。写出由有机物A制备
RCHO+RCHO(R、R代表烃基或氢原子)。写出由有机物A制备 的合成路线:_____________(无机试剂任选)。
的合成路线:_____________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,某容积恒定的密闭容器中发生如下可逆反应CO(g)+H2O(g)![]() H2(g)+CO2(g) △H>0。当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其他条件不变时,下列措施可以采用的是
H2(g)+CO2(g) △H>0。当反应达平衡时,测得容器中各物质均为n mol,欲使H2的平衡浓度增大一倍,在其他条件不变时,下列措施可以采用的是
A. 升高温度 B. 再加入2n mol H2
C. 再加入n mol CO和n mol H2O D. 再加入2n mol CO2和2n mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,ksp(CaC2O4)=2.4×10-9,下列有关0.10mol/L草酸钠(Na2C2O4)溶液的说法,正确的是
A. 溶液中各离子浓度大小关系c(Na+)>c(C2O42-)>c(HC2O4-)>c(OH-)>c(H+)
B. 若向溶液中不断加水稀释,溶液中各离子浓度均减小
C. 若用pH计测得此溶液的pH=a,则H2C2O4的第二级电离平衡常数约为Ka2=1013-2a
D. 若向该溶液中加入等体积CaCl2溶液后能够产生沉淀,则CaCl2溶液的最小浓度应该大于2.4×10-8mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A到F是化合物,且A、B、E、F均含钠元素,G是单质.

(1)写出A、B、E、F的化学式:A________,B________,E________,F________.
(2)写出反应①②③的化学方程式:① _____________________________② _________________________________③__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四个坐标图分别表示四个实验过程中某些量的变化,其中不正确的是( )

A. 向盐酸和氯化钙的混合溶液中加入碳酸钠 B. 向氢氧化钠溶液中加水
C. 双氧水分解 D. 向饱和氯化钠溶液中加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说法错误的是( )
A. 18g重甲基(-CD3)中含有的电子数为9NA
B. 22.4L(标准状况)CH2Cl2中含C-H键数为2NA
C. 10g34%H2O2溶液与足量的酸性KMnO4溶液充分反应,转移的电子数为0.2NA
D. 0.1mol由乙烯与乙醇组成的混合物完全燃烧所消托的氧气分子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为0.1 mol·L-1、体积均为100 mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg[c(H+)/c(OH-)]随加入NaOH的物质的量的变化如图所示。下列叙述正确的是( )
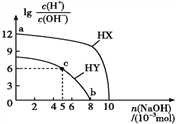
A. HX的酸性弱于HY B. c点溶液中:c(Y-)>c(HY)
C. a点由水电离出的c(H+)=10-12 mol·L-1 D. b点时酸碱恰好完全中和
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com