
| A. | 金属A在常温下能与浓硝酸反应,而B不能 | |
| B. | 金属A的阳离子的氧化性比金属B的阳离子的氧化性弱 | |
| C. | 工业上制取金属A只能用电解的方法,而金属B一般都用还原剂将其还原 | |
| D. | 将金属A和金属B用导线相连后插入某电解质溶液中构成原电池,金属A作负极 |
分析 金属的金属性越强,其最高价氧化物的水化物碱性越强、金属性较强的金属单质能置换出金属性较弱的金属单质、其单质与酸或水反应越剧烈,据此分析解答.
解答 解:A.金属A在常温下能与浓硝酸反应,而B不能,如果A是Fe、B是Mg,铁能发生钝化现象、Mg不能,所以不能说明A一定不B的金属性强,故A错误;
B.金属A的阳离子的氧化性比金属B的阳离子的氧化性弱,如氧化性Fe3+>Cu2+,但金属性Fe>Cu,所以不能说明A的金属性一定大于B,故B错误;
C.工业上用电解方法制取较活泼金属,采用氧化还原法制取较活泼金属,制取金属A只能用电解的方法,而金属B一般都用还原剂将其还原,说明A的金属性一定大于B,故C正确;
D.Mg、Al和NaOH构成的原电池中,Al易失电子作负极、Mg作正极,但金属性Mg>Al,所以不能根据原电池正负极判断金属活动性顺序,故D错误;
故选C.
点评 本题考查金属的金属性强弱判断,侧重考查元素化合物知识及原电池原理,金属的金属性强弱与失电子难易程度有关、与失电子多少无关,易错选项是BD,采用举例法解答.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题

| A. | 该方案能够计算出“钾泻盐”中KCl的质量分数 | |
| B. | 足量Ba(NO3)2溶液是为了与MgSO4充分反应 | |
| C. | “钾泻盐”化学式中x=3 | |
| D. | 上述实验数据的测定利用学校实验室里的托盘天平即可完成 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
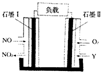 以NO、O2,熔融NaNO3,组成的燃料电池装置如图所示,在使用过程中石墨I生成NO2,Y为一种氧化物,下列说法不正确的是( )
以NO、O2,熔融NaNO3,组成的燃料电池装置如图所示,在使用过程中石墨I生成NO2,Y为一种氧化物,下列说法不正确的是( )| A. | 石墨Ⅱ电极为正极 | |
| B. | Y为N2O5 | |
| C. | 石墨Ⅰ电极方程式为NO+O2--2e-=NO2 | |
| D. | 不能用NaNO3水溶液代替熔融NaNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验方案 | 实验现象 |
| ① | 将少量氯水滴入盛有少量NaBr溶液的试管中,振荡;再滴入少量四氯化碳,振荡 | 加入氯水后,溶液由无色变为橙色,滴入四氯化碳后,水层颜色变浅,四氯化碳层(下层)变为橙红色 |
| ② | 将少量溴水滴入盛有少量KI溶液的试管中, 振荡;再滴入少量四氯化碳,振荡 | 加入溴水后,溶液由无色变为褐色,滴入四氯化碳后,水层颜色变浅,四氯化碳层(下层)变为紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同系物具有相同的最简式 | |
| B. | 同系物之间相对分子质量相差14或14的整数倍 | |
| C. | 同系物符合同一通式 | |
| D. | 同系物的化学性质基本相似,物理性质随碳原子数的增加呈规律性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 其他条件不变时,升高温度,化学反应速率加快 | |
| B. | 其他条件不变时,增大浓度,化学反应速率加快 | |
| C. | 化学反应达到反应限度时,反应物的浓度与生成物的浓度相等 | |
| D. | 化学反应的限度是不可以改变的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性 | |
| B. | 向某溶液中加入氯化钡溶液和稀硝酸,生成白色沉淀,则原溶液一定含有SO42- | |
| C. | 常温下,将铜放入浓硫酸中无明显变化,说明铜在冷的浓硫酸中钝化 | |
| D. | 浓硝酸在光照下变黄,证明硝酸不稳定,且产物有红棕色气体可溶于浓硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com