
【题目】下列离子方程式正确的是
A. 甲酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O
B. 醋酸溶液与Cu(OH)2:2CH3COOH+Cu(OH)2=Cu2++2CH3COO-+2H2O
C. 苯酚钠溶液通少量CO2 :2C6H5O-+CO2+H2O→2C6H5OH+CO32-
D. 甲醛溶液与足量的银氨溶液共热:HCHO +4Ag(NH3)2++4OH-![]() CO32-+2NH4++4Ag↓ +6NH3+2H2O
CO32-+2NH4++4Ag↓ +6NH3+2H2O
【答案】BD
【解析】
A项、甲酸为弱酸,甲酸与碳酸钠溶液反应生成甲酸钠、二氧化碳和水,反应的离子方程式为2HCOOH+CO32-=2HCOO—+CO2↑+H2O,故A错误;
B项、醋酸为弱酸,醋酸与氢氧化铜反应生成醋酸铜和水,反应的离子方程式为2CH3COOH+Cu(OH)2=Cu2++2CH3COO-+2H2O,故B正确;
C项、碳酸酸性大于苯酚,苯酚的酸性大于HCO3-,苯酚钠溶液中通入少量二氧化碳生成苯酚和NaHCO3,反应的离子方程式为C6H5O-+CO2+H2O→C6H5OH+HCO3-,故C错误;
D项、甲醛溶液与足量的银氨溶液共热发生银镜反应生成碳酸铵、银、氨气和水,反应的离子方程式为HCHO +4Ag(NH3)2++4OH-![]() CO32-+2NH4++4Ag↓ +6NH3+2H2O,故D正确。
CO32-+2NH4++4Ag↓ +6NH3+2H2O,故D正确。
故选BD。


科目:高中化学 来源: 题型:
【题目】下表是实验室制备气体的有关内容:
编号 | 实验内容 | 实验原理 |
① | 制氧气 | H2O2→O2 |
② | 制氨气 | NH4Cl→NH3 |
③ | 制氯气 | HCl→Cl2 |
(1)上述气体中:从制备过程看,必须选择合适的氧化剂才能实现的是_________(填气体的化学式,下同);从反应中有无电子转移的角度看,明显不同于其他气体的是______,写出实验室制取该气体的化学方程式_______________________________
(2)若用上述装置制备NH3,则选择的试剂为____________________。
(3)制备Cl2需用8 mol/L的盐酸100mL,现用12 mol/L的盐酸来配制。
①需要12 mol/L的盐酸的体积为__________mL(精确到0.1 mL)
②在容量瓶的使用方法中,下列操作不正确的是_______________(填写标号)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时用量筒量取浓盐酸后用玻璃棒引流入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用胶头滴管滴加蒸馏水直到凹液面的最低处和标线相平
D.定容后盖好瓶塞,用食指顶住,用另一只手手指托住瓶底,把容量瓶倒转和摇动多次
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯跟一卤代烷在催化剂作用下,可生成苯的同系物。如甲苯的制备,在催化剂作用下:![]() +CH3Cl
+CH3Cl![]() +HCl苯和下列各组物质合成乙苯最好应选用的是( )
+HCl苯和下列各组物质合成乙苯最好应选用的是( )
A.CH3 CH3和Cl2B.H2C=CH2和HCl
C.H2C=CH2和Cl2D.CH3 CH3和HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱金属元素和卤族元素广泛存在,用化学用语回答下列问题。
(1)氢氟酸可以用来雕刻玻璃。用电子式表示氟化氢的形成过程__________。
(2)过氧化钠可以用于潜水艇中氧气的来源,其与二氧化碳反应的化学方程式是_____。
(3)次氯酸钠溶液(pH>7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是_____________________。
(4)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。组装该电池必须在无水条件下进行,原因是_____________(用化学方程式表示)。
(5)关于碱金属和卤族元素,下列说法一定正确的是____________。
A.从上到下,单质密度依次增大 B.从上到下,单质熔沸点依次升高
C.从上到下,原子半径依次增大 D.单质都可以与水反应
(6)常温下,KMnO4固体和浓盐酸反应产生氯气。为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
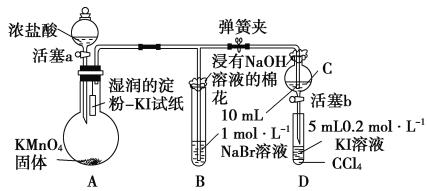
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
①验证氯气的氧化性强于碘的实验现象是____________________。
②B中溶液发生反应的离子方程式是__________________________。
③为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是___________。
(2)反应后,装置B中发生的现象是反应的离子方程式为____________;装置C中的现象是___________,表现了SO2的________ 性;装置D中现象是____________,发生反应的化学方程式为_____________________。
(3)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象____。
(4)F装置的作用是________________漏斗的作用是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有Ⅰ~Ⅳ四个体积均为0.5 L的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入HCl和O2(如下表),加入催化剂发生反应4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
2Cl2(g)+2H2O(g);ΔH,HCl的平衡转化率(α)与Z和温度(t)的关系如图所示。下列说法正确的是( )
容器 | 起始时 | ||
t/℃ | n(HCl)/mol | Z | |
Ⅰ | 300 | 0.25 | a |
Ⅱ | 300 | 0.25 | b |
Ⅲ | 300 | 0.25 | 4 |
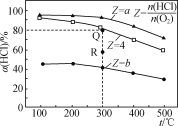
A. ΔH<0,a<4<b
B. 300℃该反应的平衡常数的值为64
C. 容器Ⅲ某时刻处在R点,则R点的υ正>υ逆,压强:p(R)>p(Q)
D. 若起始时,在容器Ⅳ中充入0.25molCl2和0.25molH2O(g),300℃达平衡时容器中c(HCl)=0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和限度的说法中,不正确的是( )
A.实验室用H2O2分解制O2,加入MnO2作催化剂后,反应速率明显加快
B.2SO2+O2![]() 2SO3反应中,SO2的转化率能达到100%
2SO3反应中,SO2的转化率能达到100%
C.日常生活中用冰箱冷藏食物可降低食物变质的反应速率
D.可逆反应在一定条件下达到化学反应限度时正反应速率和逆反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是
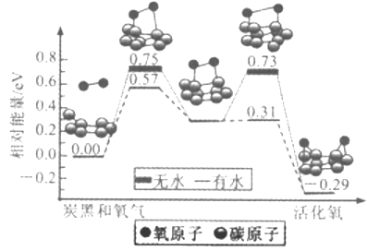
A. 氧分子的活化包括O-O键的断裂与C-O键的生成
B. 每活化一个氧分子放出0.29eV的能量
C. 水可使氧分子活化反应的活化能降低0.42eV
D. 炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,向100 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图所示。下列分析正确的是

A. a点对应溶液的导电性比d点强
B. 氢硫酸的酸性比亚硫酸的酸性强
C. 向d点对应的溶液中加入Ba(NO3)2溶液,产生BaSO4白色沉淀
D. H2S饱和溶液的物质的量浓度为0.05 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com